
题目列表(包括答案和解析)
12.D解析:A表现了HNO3的氧化性;B表现了HNO3的酸性;C主要表现HNO3的不稳定性。
11.AC 解析:设两气体恰好完全反应,则由反应方程式:
6NO2+8NH3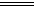 7N2+12H2O
7N2+12H2O
6 8



 -
- ≠2,故不可能是此种情况。
≠2,故不可能是此种情况。
①若NO2过量,NH3完全反应,设 =
= mL,则反应的NO2体积为(
mL,则反应的NO2体积为( -2)mL,应有(
-2)mL,应有( -2)∶=6∶8,解得
-2)∶=6∶8,解得 =8mL,故
=8mL,故 (NO2):
(NO2): (NH3)=12:8=3:2。
(NH3)=12:8=3:2。
②若NH3过量,NO2完全反应,设 (NO2)=
(NO2)= mL,则反应的NH3为(
mL,则反应的NH3为( +2)mL,应有
+2)mL,应有 :(
:( +2)=6:8,解得
+2)=6:8,解得 =6mL,故
=6mL,故 (NO2):
(NO2): (NH3)=6∶14=3∶7
(NH3)=6∶14=3∶7
10.B解析:依题意,NH -OH--NH3↑SO
-OH--NH3↑SO -Ba2+-BaSO4↓
-Ba2+-BaSO4↓
 mol
mol  mol
mol  mol
mol  mol
mol
即混合溶液中含(NH4)2SO4为2 mol,其电离产生NH
mol,其电离产生NH 4
4 mol,则原混合溶液中NH4NO3的物质的量为(2
mol,则原混合溶液中NH4NO3的物质的量为(2 -4
-4 )mol,所以,
)mol,所以, (NO
(NO )=
)= mol·L-1,答案选B。
mol·L-1,答案选B。
9.B解析:水充满烧瓶,则所得溶液的体积相同且都等于烧瓶的容积。又因为NH3和HCl的体积相同,物质的量也相同,故溶液的物质的量浓度之比为1∶l。
8.A解析:氨水的浓度为 mol·L-1
mol·L-1
7.A解析:氨气溶于水形成氨水,其溶质为氨气。设烧瓶的容积为 L,则形成溶液的体积为
L,则形成溶液的体积为 L,溶质的物质的量为
L,溶质的物质的量为 mol,故所得溶液的物质的量浓度为
mol,故所得溶液的物质的量浓度为 =0.045mol·L-1
=0.045mol·L-1
6.D
5.C解析:A组中SO2不能用碱石灰干燥。B组均不能用碱石灰干燥的气体。D组均可用浓H2SO4作干燥剂,但其中SO2、Cl2不能用碱石灰干燥。
4.B解析:设各取体积为 L,90%H2SO4密度为
L,90%H2SO4密度为 ,10%H2SO4密度为
,10%H2SO4密度为 ,则
,则 >
> 。依题意,混合后溶液的百分比浓度
。依题意,混合后溶液的百分比浓度 %=
%=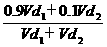 =
= %=
%=
所以 %>50%,选B。
%>50%,选B。
3.BC解析:Cu+2H2SO4(浓) CuSO4+SO2↑十2H2O
CuSO4+SO2↑十2H2O
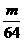 mol
mol  mol
mol
参加反应的Cu,生成的SO2与被还原的H2SO4的物质的量相等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com