
题目列表(包括答案和解析)
2.实验室保存下列试剂,其中保存方法和理由描述都正确的是 ( )
|
编号 |
试 剂 |
保存方法 |
理 由 |
|
A |
固体氢氧化钠 |
存放在带橡皮塞的广口瓶中 |
防止空气接触被氧化,防止和水蒸气、二氧化碳接触而变质 |
|
B |
碳酸钠晶体 |
存放在干燥密封的广口瓶中 |
防止风化成粉末而变质 |
|
C |
液溴 |
存放在带橡皮塞的细口瓶中 |
防止挥发 |
|
D |
硝酸银溶液 |
存放在无色玻璃塞的试剂瓶 中,放在冷暗处 |
防止见光分解 |
1.广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置,下图中能用作安全瓶防倒吸的装置是( )
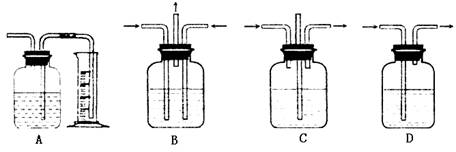
可能用到的原子量:H 1 C 12 O 16 S 32 Mg 24 Ca 40 Cl 35.5 Na 23
14.(每空3分,共15分)W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
⑴ W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为
_______________________________________________________________________。
⑵ W与Y 可形成化合物W2Y,该化合物的电子式为______________。
⑶ Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
_______________________________________________________________________。
⑷ 比较Y、Z气态氢化物的稳定性由强到弱的顺序是(用分子式表示)______________
⑸ W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示):
_______________________________________________________________________。
13.(每空3分,共15分)已知四种元素A、B、C、D,其原子序数依次增大,最外层电子依次为4、1、2、7,其中A元素原子次外层电子数为2,B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,D元素的单质为液态非金属单质。若此四种元素均位于元素周期表前四个周期,按要求填写下列各题:
⑴ A元素的气态氢化物用电子式表示为_______________________________,
D元素在周期表中的位置为_____________________________________。
⑵ B元素的最高价氧化物的水化物用电子式表示为
⑶ C、D两元素形成的化合物属于__________化合物,用电子式表示其生成过程为
_____________________________________________________________________。
12.(每空1分,共14分)动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
|
实验步骤 |
实验现象 |
|
① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
|
② 向新制得的Na2S溶液中滴加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
③ 将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体 |
|
④ 将镁条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
|
⑤ 将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
|
⑥ 向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉淀。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:
研究 元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,
NaOH溶液,酚酞溶液等。
仪器和用品:① ,② ,③ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:
(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
|
实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
|
实验现象(填A~F) |
|
|
|
|
|
|
① ,② ,
(4)此实验的结论: , 。
11.(每空2分,共16分)下表是元素周期表的一部分,请回答有关问题:

|
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式 。
(3)④元素与⑦元素形成化合物的电子式 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)在⑦与⑩的单质中,化学性质较活泼的物质名称是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。
10.X、Y、Z是三种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )
A.元素非金属性由弱到强的顺序为X<Y<Z
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.三种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
9.元素在周期表中的位置,反映了元素的原子结构和 元素的性质,下列说法正确的是
元素的性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
8.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是:
A.CO2的电子式: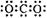 B.质量数为37的氯原子:1737Cl
B.质量数为37的氯原子:1737Cl
 C.NH4Cl的电子式: D.原子核内有10个中子的氧原子:
C.NH4Cl的电子式: D.原子核内有10个中子的氧原子:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com