
题目列表(包括答案和解析)
10. 某元素最高价氧化物对应水化物的化学式是H2XO3,该元素的气态氢化物的化学式为
A.HX B.H2X C.XH3 D.XH4
9.能够说明硫的非金属性比氯弱的事实有( )
①Cl2与铁反应生成FeCl3,S与铁反应生成FeS ② Cl2和H2的混合气,经强光照射可剧烈反应,而S与H2反应需较高温度 ③ 将Cl2通入氢硫酸中可置换出硫 ④ 常温时硫单质为固态而氯单质为气态。
A.①③ B.①②③ C.②④ D.①②③④
8.某主族元素R的最高正化合价与最低负化合价的代数和为2,由此可以判断( )
A.R一定是第四周期元素 B.R一定是ⅣA族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定 D.R气态氢化物化学式为RH3
7.下列各组化合物的性质比较中不正确的是( )
A、酸性:HClO4>HBrO4>HIO4 B、碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
C、稳定性:HCl>H2S>PH3 D、原子半径:N<O<S
6.下列有关离子键、共价键的叙述中正确的是( )
A、离子化合物中只存在离子键,没有共价键
B、非极性键只存在于双原子的单质分子中
C、共价化合物分子中一定不存在离子键
D、仅由非金属元素组成的化合物中一定不含离子键
5、对下列几种微粒:①13 6C;②3919K;③4020Ca;④12 6C;⑤4018Ar的有关说法不正确的是( )
A、①、④互为同位素 B、③、⑤的质量数相等
C、②、③的中子数相等 D、1 mol③与1 mol⑤的质量相等
4.下列说法错误的是( )
A.只要发生化学键断裂的变化,则一定是化学变化
B.熔、沸点:CF4<CCl4<CBr4<CI4
C.氢键不是一种化学键,而是一种分子间作用力
D.水结冰时体积膨胀、密度减小就是因为氢键的存在
3.下列物质的晶体中,既含有离子键,又含有非极性共价键的是( )
A.NaOH B.Na2O2 C.CaCl2 D.H2O2
1、石材的放射性常用镭(226 88Ra)作为标准,居里夫人因对Ra元素的研究曾两度获得诺贝尔奖。下列有关镭(226 88Ra)的叙述中不正确的是( )
A、226 88Ra原子核内有138个中子 B、226 88Ra原子核外有88个电子
C、226 88Ra原子核内有88个质子 D、Ra元素位于第三周期
 2.下列表达方式错误的是( )
2.下列表达方式错误的是( )
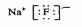 A.甲烷的电子式: B.氟化钠的电子式:
A.甲烷的电子式: B.氟化钠的电子式:
C.硫离子的电子式:S2-
D.碳-12原子: C
C
25.某元素最高价氧化物的化学式是RO2,已知其气态氢化物中含氢25%。
(1)计算R的相对原子质量(2分);
(2)写出R最高价氧化物对应的水化物的化学式(1分),并设计一个实验方案证明其
酸性比盐酸弱。(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com