
题目列表(包括答案和解析)
27.(8分)现有一份CuO和Cu2O混合物,用H2还原法测定其中CuO的质量x(g)。实验中可以测定如下数据:w-混合物的质量(g)、w(H2O)-生成H2O的质量(g)、w(Cu)-生成Cu的质量(g)、V(H2)-消耗的H2的体积(L)。
⑴为了计算x,至少需要测定上述四个数据中的______个,这几个数据的组合共有_____种,请将这些组合一一填入下表空格中。
说明:①选用w、w(H2O)、w(Cu)、V(H2)表示,不必列出具体计算式。
②每个空格中填一种组合,有几种组合就填几种,不必填满。
⑵从上述组合中选写一个含w的求x的计算式:x=____________________。
26.(3分)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2:1,则该混合物中含CaCl2的质量分数为__________,KCl与CaCl2的物质的量之比为_________,含1molCl-的该混合物的质量是__________g。
25.(1分)在28%的KOH水溶液中,OH-与水分子数之比是____________。
24.(2分)标准状况下,2gH2与16gO2混合后,其体积是__________L,密度是________g/L。
23.(7分)为了测定某气体样品C4H10(并含有少量C3H8,均不溶于水)的平均相对分子质量,设计了下面的实验:
①取一个配有合适胶塞的洁净、干燥的锥形瓶,准确称量,得到质量m1;
②往锥形瓶中通入干燥的该气体样品,塞好胶塞,准确称量,重复操作,直至前后两次称量结果基本相同,得到质量m2;
③往锥形瓶内加满水,塞好胶塞,称量,得到质量m3。
已知实验时的温度为T(K),压强为p(kPa),水的密度为ρ水(g/L),空气的相对平均分子质量为29.0,密度为ρ空气(g/L)。回答下列问题:
⑴本实验的原理是(具体说明)_________________________________________________。
⑵步骤②中为什么要重复操作,直至前后两次称量结果基本相同?
答:______________________________________________________________________。
⑶具体说明本实验中怎样做到每次测量都是在相同体积下进行的?
答:______________________________________________________________________。
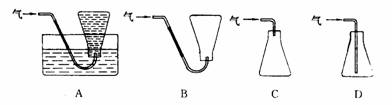
⑷本实验中收集气体样品的操作,可选用的方法是(填下图中标号)___________。
⑸锥形瓶中空气的质量(m空气)是___________________________(列出算式)。
⑹锥形瓶中样品的质量(m样品)是___________________________(列出算式)。
⑺由实验测得该气体样品的平均相对分子质量是________________________(列出算式)。
22.将50mLH2、CO和CO2的混合气体,与20mLO2(过量)于某容器中混合,引燃后冷却,当恢复至原室温时,测得气体体积为37mL,通过NaOH溶液后剩余的气体为3mL,则原50mL混合气体中CO2、CO、H2的体积(mL)依次是 ( )
A. 16、16、18 B. 16、18、16 C. 18、16、16 D. 18、14、18
21.X2气和Y2气共100mL,通过光照使它们充分反应,恢复到原状况时,发现体积仍是100mL,这说明 ( )
A. X2气过量 B. X2气和Y2气各50mL
C. 产物是双原子分子 D. 无法作出上述判断
20.1L甲气体和1L乙气体恰好完全反应生成2L丙气体(所有气体的体积均在标准状况下测定)。若丙气体的分子式是YX2,则甲、乙的分子式分别是 ( )
A. X2和Y2 B. XY和Y2 C. X2和XY D. YX2和Y2
19.已知阿伏加德罗常数、物质的摩尔质量及摩尔体积,尚不能全部计算出其近似值的物理量是 ( )
A. 固体物质分子的大小和质量 B. 液态物质分子的大小和质量
C. 气体物质分子的大小和质量 D. 气体物质分子的质量
18.在标准状况下,下列气体混合后所得混合气体的平均相对分子质量可能为40的是
( )
A. H2和O2 B. F2和HCl C. SO2和HBr D. N2和Cl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com