
题目列表(包括答案和解析)
32.(8分)某学生用0.10mol/L的KOH标准溶液滴定未知浓度的盐酸,其操作有如下几步:
①取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞;
②用标准溶液润洗滴定管2-3次;
③把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
④取标准KOH溶液注入碱式滴定管至刻度0以上2-3cm;
⑤调节液面至0或0以下刻度,记下读数;
⑥把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。就此实验完成填写:
(1)正确操作步骤的顺序是(用编号填写)________→①→⑥;
(2)判断到达滴定终点的实验现象是________________;
(3)滴定达终点后,用去KOH标准溶液18.48mL,计算盐酸的物质的量浓度为________;
(4)试分析,下列实验操作造成实验结果偏低的原因可能是________(选填字母序号)。
A.步骤②中,未用标准溶液润洗滴定管;
B.用来配制标准溶液的KOH固体中含少量NaOH;
C.滴定时,锥形瓶摇动太激烈,有少量液体溅出;
D.滴定到终点时,滴定管尖嘴悬有液滴;
E.读碱式滴定管开始时仰视,读终点时俯视。
31.(6分)按要求填空:
(1)将pH=11的氨水和pH=3的盐酸等体积混合,所得溶液中所有离子浓度由大到小的顺序为________________。
(2)常温下,pH=13的Ba(OH)2溶液a L与pH=3的H2SO4溶液b L混合(混合后溶液体积变化忽略不计),若所得混合溶液pH=12,则a:b=________。
(3)已知某溶液中只存在 、
、 、
、 、
、 四种离子,实验测得
四种离子,实验测得
 ,则该溶液中溶质为________。
,则该溶液中溶质为________。
30.(8分)溶质质量分数为63%的浓硝酸,密度为1.40g/cm3。试计算(写出计算过程):
(1)该浓硝酸的物质的量浓度是多大?
(2)欲用浓硝酸配制500mL 2.0mol/L的稀硝酸,需取用上述浓硝酸多少mL?
(3)取配制好的溶液40mL,与足量铜充分反应,最多可生成气体(标况下)多少?
注意:310-33题为13、14班同学题目,1-12班同学不做
29.(12分)A、B、C、D、E五瓶透明溶液,分别是盐酸、氯化钡、硫酸氢钠、碳酸钠和硝酸银中的一种,已知:
(1)A与B反应有气体生成;
(2)B与C反应有沉淀生成
(3)C与D反应有沉淀生成;
(4)D与E反应有沉淀生成
(5)A与E反应有气体生成;
(6)在(2)和(3)的反应中生成的沉淀是同一种物质。
请填空:(1)在(2)和(3)的反应中,生成的沉淀物质的化学式(分子式)是________。
(2)B是________;C是________;D是________;E是________。
(3)A与E反应的离子方程式是________。
28.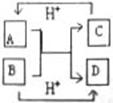 (10分)已知A、B、C、D是中学化学中常见的四种不同微粒。它们 之间存在如右所示的转化关系:
(10分)已知A、B、C、D是中学化学中常见的四种不同微粒。它们 之间存在如右所示的转化关系:
(1)如果A、B、C、D均是含10个电子的微粒,请写出A的化学式________; D的电子式________。
(2)如果A和C是含18个电子的微粒,B和D是含10个电子的微粒。 请写出:
①A和B在溶液中反应的离子方程式________________
②根据上述离子方程式,可以判断C与B结合质子的能力大小是(用化学式或离子符号表示):________ ________。
注意:29、30两题为1-12班同学题,13、14班同学不做。
27.(10分)下面是实验室制取NH3的装置和选用的试剂,根据要求填写空白。

(1)实验室用A装置制备干燥的NH3:
①反应的化学方程式为:________________。
②装置中收集NH3的试管口放置棉花团的作用是:________________。
(2)实验室用B装置快速制取较大量NH3。
①用化学方程式表示,浓氨水滴入CaO中有大量NH3逸出的过程:________。
②检验NH3是否收集满的实验方法是:________________。
③假定在标准状况下作NH3喷泉实验,烧瓶中所得溶液的物质的量浓度是________mol/L。
26.(10分)书写下列化学方程式
(1)氮气和氢气合成氨的反应________________
(2)浓硫酸与铜的反应:____________________
(3)稀硝酸与铜的反应:____________________
(4)浓硝酸与铜的反应:____________________
(5)二氧化硅与碳在高温下的反应:__________
25.能正确表示下列化学反应的离子方程式是( )
A.用碳酸钠溶液吸收少量二氧化硫:
B.金属铁溶于稀硝酸中:
C.NH4HCO3和过量NaOH溶液混和共热:


D.碳酸钙溶于硝酸中:
第Ⅱ卷
24.同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2,现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为 、
、 、
、 ,则下列关系正确的是( )
,则下列关系正确的是( )
A. B.
B. C.
C.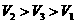 D.
D.
23.下列各组离子因发生氧化-还原反应而不能大量共存的是( )
A. 、
、 、
、 、
、 B.
B. 、
、 、
、 、
、
C. 、
、 、
、 、
、 D.
D. 、
、 、
、 、
、
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com