
题目列表(包括答案和解析)
29.(10分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,标况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
|
时间(min) |
1 |
2 |
3 |
4 |
5 |
|
氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0-1、1-2、2-3、3-4、4-5 min)反应速率最大 ,
原因是 。
(2)哪一段时段的反应速率最小 ,原因是
。
(3)求2-3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,要写出计算过程)
。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号) 。
28、(11分)每空一分
|
A |
|
|
|||||||||||||||||||||||
|
B |
|
|
|
C |
D |
E |
F |
|
|||||||||||||||||
|
G |
|
H |
|
|
|
I |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
(1)在上面元素周期表中全部是金属元素的区域为 。
(A)a (B)b (C)c (D)d
(2)G元素与 E元素形成的化合物的化学式是 、 ,它们都是
(填“共价化合物”或“离子化合物”)。表格中十种元素的最高价氧化物对应的水化物中,碱性最强的是 (用化合物的化学式表示,下同),酸性最强的是 ,属于两性氢氧化物的是 。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是 。(填编号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
27、(8分)(1)用电子式表示H2O和MgBr2的形成过程 。
(2) H2O以 键结合,MgBr2以 键结合。(填极性键、非极性键、离子键)
(3)
14CO2与碳在高温条件下发生反应:14CO2+C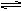 2CO,该反应是 热反应,达到平衡后,平衡混合物中含14C的粒子有
2CO,该反应是 热反应,达到平衡后,平衡混合物中含14C的粒子有
26.已知一定温度下,N2 和H2 反应生成2mol NH3时放出的热量为92.0 kJ, 此温度下的
1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为( )[忽略能量损失]
A.一定大于92.0 kJ B. 一定等于92.0 kJ C. 一定小于92.0 kJ D. 不能确定
第Ⅱ卷 (非选择题 共51分)
25.有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:( )
A.A>B>C>D B.C>A>B>D C.A>C>D>B D.B>D>C>A
24. X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是 ( )
A.R一定是共价化合物
B.R一定是离子化合物
C.R可能是共价化合物,也可能是离子化合物
D.R可能是气态物质,也可能是固态物质
23.下列关于碱金属的叙述正确的是 ( )
A、钾与氧气或水反应比钠的反应剧烈,铷、铯的反应更剧烈
B、碱金属的密度 随着原子序数的递增逐渐减小
C、碱金属元素的最高价氧化物对应的水化物 的碱性随着原子序数的递增依次增强
D、碱金属元素的阳离子的氧化性 随着原子序数的递增 依次增强
22.氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应如下:2H2+4OH--4e-==4H2O O2+2H2O+4e-==4OH-
下列说法错误的是( )
A.氢气通入正极,氧气通入负极
B.燃料电池的能量转化率不能达到100%
C.供电时的总反应为:2H2+O2 ==== 2H2O
D.产物为无污染的水,属于环境友好电池
21.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是 ( )
|
X |
Y |
|
|
|
Z |
W |
A.原子半径: W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.四种元素的单质中,Z单质的熔、沸点最高
D.W的单质能与水反应,生成一种具有漂白性的物质
20、已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均是具有相同电子层结构的短周期元素形成的简单离子,下列说法正确的是( )。
A.原子半径C>D>A>B B.原子序数b>a>c>d
C.离子半径D>C>A>B D.单质的还原性A>B>C>D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com