
题目列表(包括答案和解析)
8. 已知离子 bX 3+ 的原子结构示意图为: 。下列认识正确的是( )
已知离子 bX 3+ 的原子结构示意图为: 。下列认识正确的是( )
A.b=10
B.X单质能溶于氢氧化钠溶液
C.X为稀有气体
D.X单质既具有还原性,又具有氧化性
7.实际存在的 H、
H、 H、
H、 H、H+和H2,它们是( )
H、H+和H2,它们是( )
A.氢的五种同位素 B.五种氢元素
C.氢的五种原子 D.氢元素的五种不同微粒
6.某元素原子的最外电子层上只有2个电子,该元素是( )
A.一定是IIA元素 B.一定是金属元素
C.一定是+2价元素 D.可能是金属元素,也可能是非金属元素
5.下列叙述中错误的是( )
A.原子半径:O<Cl<S B.稳定性:HF<HCl<HBr
C.还原性:Na>Mg>Al D.酸性:HClO4>H2SO4>H3PO4
4.下列微粒半径之比大于1的是( )
A. B.
B.
C. D.
D.
3.某元素原子核外有三层电子,其最外层电子数是次外层电子数的一半,则此元素是( )
A.S B.C C.Si D.P
2.据科学家预测,月球的土壤中吸附着数百万吨的3 2He,每百吨3 2He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以4 2He的形式存在。下列说法正确的是( )
A.4 2He原子核内含有4个质子
B.3 2He和4 2He互为同位素
C.3 2He原子核内含有3个中子
D.4 2He的最外层电子数为2,所以4 2He具有较强的金属性
1.下列粒子的结构示意图正确的是( )


22.(7分)一定量的铜与500 mL 18.4mol/L(足量)浓硫酸充分反应,已知有0.5 mol H2SO4被还原。请回答下列问题:
(1)生成的气体在标准状况下的体积为_________________。
(2)所得溶液中Cu2+的物质的量浓度为(假设反应前后溶液体积不变)_________________。
(3)将上述反应后的溶液稀释后加入足量的Zn粒,计算参加反应的Zn粒的质量为__________。
22.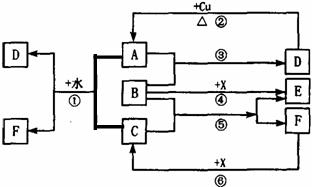 (8分)已知A-F是中学化学中常见物质,其中常温下A、C、E、F为气体,B、D为液体,A是一种大气污染物,可形成酸雨,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。
(8分)已知A-F是中学化学中常见物质,其中常温下A、C、E、F为气体,B、D为液体,A是一种大气污染物,可形成酸雨,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。
试回答下列问题:
(1)B的结构式为 。
(2)写出反应②的化学方程式 。
(3)写出反应①的离子方程式_______________________________。
(4)由图中所给反应关系判断B、C、D、X氧化性从强到弱的顺序是 __ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com