
题目列表(包括答案和解析)
3.对于 A ZX 和A+1 ZX+ 两种粒子,下列叙述正确的是
A.质子数一定相同,质量数和中子数一定不同
B.化学性质几乎相同
C.一定都由质子、中子、电子构成
D.核电荷数,核外电子数一定相同
2.某粒子含有6个质子,7个中子,电荷为0,则它的化学符号是
A. 13Al B.13Al C.13 C D. 13C
1.提出元素周期律并根据周期律编制第一个元素周期表的科学家是
A.道尔顿 B.普利斯特里 C.门捷列夫 D.阿佛加德罗
34.(10分)红磷P(S)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)
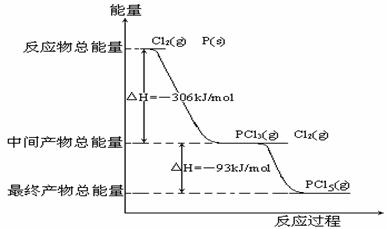
根据上图回答下列问题
(1)P和Cl2反应生成PCl3的热化学方程式 ;
(2)PCl5分解生成PCl3和Cl2的热化学方程式 ;
(3)P和Cl2分两步反应生成1mol PCl5的△H3= ;P和Cl2一步反应生成1mol PCl5的△H4 △H3(填“大于”,“小于”或“等于”); K^S*5U.
33.(8分)甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇
(1)将1mol CH4和2mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ
CO(g)+3H2(g)……Ⅰ
①已知100℃达到平衡时,CH4的转化率为50%,达到平衡所需的时间为5min,则用H2表示的平均反应速率为__ __。
②在其它条件不变的情况下降低温度,反应速率将___ _ (填“增大”、“减小”或“不变”)。
(2)在压强为0.1 MPa条件下, 将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)  CH3OH(g) ……Ⅱ。
CH3OH(g) ……Ⅱ。
③该反应的△H__ _0。(填“<”、“>”或“=”)
④为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
|
l
实验编号 |
l
T(℃) |
l
n (CO)/n(H2) |
l
P(MPa) |
|
l
ⅰ |
l
150 |
l
1/3 |
l
0.1 |
|
l
ⅱ |
l
_ _ |
l
_ _ |
l
5 |
|
l
ⅲ |
l
350 |
l
_ _ |
l
5 |
请在上表空格中填入剩余的实验条件数据。
32.(6分)把6 mol A和5 mol B 混合于4升密闭容器中,发生反应:
 3A(g) + B(g) xC(g) + D(g),
3A(g) + B(g) xC(g) + D(g),
测得5分钟末达到平衡,生成1molD,又知C的平均反应速率为0.1mol ·(L·min)-1,则:
(1)x值为 ;
(2)5分钟末B的物质的量浓度为 ;
(3)A的平均反应速率为 。
31.(8分)实验室通过简单的“试管实验”,即可探索元素的金属性、非金属性的强弱。请你选用下列试剂:镁条、铝条、氯水、AlCl3溶液、MgCl2溶液、NaBr溶液、NaOH溶液。
根据实验要求完成下表
|
实验方案 (只要求填写选用试剂) |
实验现象 |
结论 |
|
|
⑴ |
|
一支试管中有白色沉淀,另一支试管中先生成白色沉淀,后白色沉淀消失。 |
金属性:Mg>Al |
|
⑵ |
|
|
非金属性: |
30.(10分)有A、B、C、D四种元素,已知:A的最高价与其负价的代数和为6;A、D次外层电子都是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B是形成化合物种类最多的元素;C2-离子与氩原子具有相同的电子层结构。试写出:
(1)各元素的符号:A ,B ,C ,D 。
(2)B的最高价氧化物的电子式为 ;
D与C形成化合物的电子式为 。
(3)A、D分别对应的最高价氧化物水化物之间反应的化学方程式 。
29.(8分)下表是元素周期表的一部分。
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
1 |
① |
|
|||||
|
2 |
|
|
|
|
② |
|
③ |
|
3 |
④ |
⑤ |
⑥ |
|
|
⑦ |
⑧ |
(1)表中原子半径最小的元素符号是 ;
(2)表中氧化性最强的单质的化学式为 ;
(3)表中最高价氧化物的水化物中碱性最强的物质的化学式是_____________;
(4)④⑤⑥三种元素中,离子半径最小的离子符号是 ;K^S*5U.
(5)③⑦⑧三种元素的气态氢化物的稳定性强弱顺序为 > > (填化学式);
(6)元素②的氢化物与元素⑧的氢化物反应的化学方程式为 。
28.(3分)1克氢气燃烧生成液态水放出142.9 kJ热量,该反应的
热化学方程式是 。K^S*5U.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com