
题目列表(包括答案和解析)
5.下列物质的电子式书写正确的是
A.NH4Cl的电子式: B.四氯化碳
B.四氯化碳 
C.氮  D.二氧化碳
D.二氧化碳 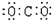
4.我国稀土资源丰富。下列有关稀土元素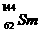 与
与 的说法正确的是
的说法正确的是
A.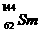 与
与 互为同位素 B.
互为同位素 B.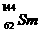 与
与 的质量数相同
的质量数相同
C.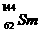 与
与 是同一种核素 D.
是同一种核素 D.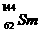 与
与 的核外电子数和中子数均为62
的核外电子数和中子数均为62
3.下列物质中,含有非极性共价键的是
A.O2 B.CO2 C.NaOH D.MgCl2
2.X元素最高氧化物对应的水化物为H2XO4,则它对应的气态氢化物的化学式为
A.HX B.H2X C.XH4 D. XH3
1.根据元素在周期表中的位置判断,下列元素中原子半径最小的是
A.硫 B.氯 C.硅 D. 磷
6.3:1
25.城市使用的燃料,现大多为煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它有煤炭与水蒸气在高温下反应制得,故又称水煤气。试回答:
(1)写出制取水煤气的主要化学方程式 ,
该反应是 反应(填吸热、放热)。(3分)
(2)设液化石油气的主要成分为丁烷(C4H10),其充分燃烧后产物为C02和H2O,试比较
完全燃烧等质量的C4H10及CO所需的氧气的质量比 (结果保留1位小数)。(4分)
答案CCBCD DCDCC CBBAA BBA
19 三 VIIA HClO4 Na Mg O Na2O
Cl2 + 2OH- = Cl- + ClO - + H2O
20 HF 共价键(极性键)
21 A D
22 ③①②
23 ①③⑥
24 1:2 1:2 2:5 1:2 1:4
25 C+ H2O = CO+ H2 吸
24、 36 g H2O与80 g D2O的物质的量之比是_ _____,分子中所含质子数之比是________,所含中子数之比是____ ___,它们分别与Na反应时,所放出气体体积之比(同条件下)是________,质量之比是________。(10分)
23.在一块大理石(主要成分是CaCO3)上,先后滴加①1mol/LHCl溶液和②0.1mol/LHCl溶液反应快的是滴加了____ _________的(填序号,下同),先后滴加同浓度的③热盐酸和④冷盐酸,反应快的是滴加 的,用⑤大理石块和⑥大理石粉分别跟同浓度的盐酸起反应,反应快的是用了 的。(6分)
22、离子键的强弱主要决定于离子半径和离子的电荷值。一般规律是:离子半径越小,电荷值越大,则离子键越强。 试分析:①K2O ②CaO ③MgO 的离子键由强到弱的顺序是 (4分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com