
题目列表(包括答案和解析)
17.下列说法中正确的是 ( )
A.化学键的断裂和形成是化学反应中能量变化的主要原因.
B.化学反应速率为0.8 mol /(L·s)是指1s 内生成0.8mol该物质.
C.化学键只能使原子相结合, 不能使离子相结合.
D.天然气﹑石油和水煤气分别属于化石能源﹑可再生能源和二次能源.
16. 右图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是 ( )
右图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是 ( )
A.B为第二周期的元素 B.C为VIA族元素
C.氢化物稳定性B > C > A D.C元素单质是化学性质最活泼的非金属
15.下列反应过程中,同时有离子键和共价键断裂和形成的是 ( )
A.2H2+O2 = 2H2O B.NH3+HCl = NH4Cl
C.8NH3+3Cl2 = 6NH4Cl+N2 D.2Na2O2+2H2O=4NaOH+O2
14.下列说法正确的是( )
A.酸与碱发生中和反应所放出的热量称为中和热。
B.化学反应中能量变化的大小与反应物的质量多少无关。
C.由1H、2H、3H、35Cl、37Cl组成的氯化氢分子有6种。
D.O2与O3的相互转化是物理变化。
13.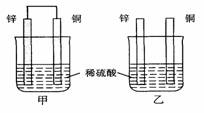 将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯的溶液中H+ 浓度均减小
D.乙装置中化学能转化为电能
12.下列反应中生成H2的速率最快的是 ( )
|
|
金属 |
酸溶液 |
温度 |
|
A |
Zn |
0.5mol·L-1 H2SO4 |
20℃ |
|
B |
Fe |
1 mol·L-1HCl |
20℃ |
|
C |
Al |
2 mol·L-1HCl |
30℃ |
|
D |
Mg |
2 mol·L-1H2SO4 |
30℃ |
11.有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,只用一种试剂就可把它们鉴别开来,这种试剂是 ( )
A.盐酸 B.烧碱溶液 C.氨水 D.KSCN溶液
10.将N2和H2置于2L密闭容器中,反应2min后,生成0.8molNH3。在这段时间内,用N2浓度变化表示的反应速率为( )
A.0.01mol·L-1·min-1 B.0.2mol·L-1·s-1 C.0.1mol·L-1·min-1 D.0.4mol·L-1·s-1
9.在密闭容器中,存在反应:2SO2(g)+O2(g) 2SO3(g),下列可使化学反应速率增大的措施是 (
)
2SO3(g),下列可使化学反应速率增大的措施是 (
)
A.减少SO2浓度 B.升高温度 C.增大容器体积 D.降低温度
8.下列各组顺序的排列不正确的是 ( )
A.还原性:I->Br->Cl- B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H4SiO4<H2CO3<HNO3 D.碱性:NaOH>Mg(OH)2>Ca(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com