
题目列表(包括答案和解析)
3.以下关于元素周期表的结构叙述正确的是
A.元素周期表有七个主族,八个副族
B.元素周期表有三个长周期(均含18种元素),三个短周期(均含8种元素)
C.第三主族位于元素周期表的第三列(从左往右)
D.零族位于元素周期表的第18列(从左往右)
2.一些简单原子的原子结构可用下图①、②、③形象地表示:

根据该图的示意,则下列有关图①、②、③所表示的原子叙述正确的是
A.①②③互为同位素 B.①②③为同素异形体
C.①②③为同种原子 D.①②③具有相同的质量数
1.同周期ⅠA和 ⅢA族两种元素原子的核外电子数的差值不可能为
A.2 B.12 C.18 D.26
32. A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同一主族元素,B、D元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,B,C可形成C2B,C 2 B 2两种化合物,且、又知四种元素的单质中有两种气体、两种固体。请回答:
(1)D在周期表中的位置 周期 族
(2)写出由ABC三元素形成的化合物的电子式:
(3)D的单质能跟C的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式____________ _______。
(4)A、B、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 。
31. (8分)
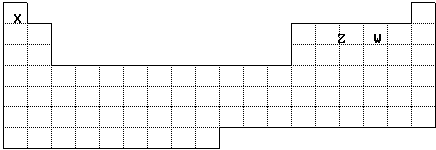
已知X、Y、Z、W、M五种元素,X、Z、W在元素周期表位置如上周期表,① ZX4+ + WX-
= ZX3 + X2W,且反应物和产物中各微粒的电子总数与M3+相等②Z2与YW分子中质子数
相等。回答下列问题:
(1)在周期表中写出M、Y的元素符号;
(2)写出ZX3的电子式: ;
(3)写出M单质与NaOH溶液反应的离子方程式 ;
(4)M的最高价氧化物对应水化物与Z的最高价氧化物对应的水化物反应的化学方程式为: 。
选作题(10分)
30.(6分)氧化还原反应中除了原子守恒(质量守恒)外,氧化剂得电子总数和还原剂失电子总数相等,在一定条件下,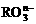 和I-发生反应的离子方程式为:
和I-发生反应的离子方程式为:
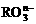 +6I-+6H+=R-+3I2+3H2O(R为主族元素)则:
+6I-+6H+=R-+3I2+3H2O(R为主族元素)则:
(1)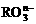 中R的化合价为 价,n值为 。
中R的化合价为 价,n值为 。
(2)R元素最外层电子数为 个,在周期表的 族。
29.(8分)实验探究是体验知识的产生和形成过程的基本途径。下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
请回答:
|
实验步骤 |
实验结论 |
|
①氯水+1 mL
CCl4,振荡,静置,观察四氯化碳层颜色 |
氧化性从强到弱的顺序:氯、溴、碘 |
|
②NaBr溶液+氯水+1 mL
CCl4,振荡,静置,观察四氯化碳层颜色 |
|
|
③KI溶液+氯水+1 mL
CCl4,振荡,静置,观察四氯化碳层颜色 |
(1)完成该实验需用到的实验仪器是 。
(2)CCl4在实验中所起的作用是 。
(3)该同学的实验设计不足之处是 ,改进的办法是 。
28.(10分)a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: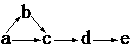
其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物。
(1)如果a是一种淡黄色粉末固体,试推断这五种物质(用名称表示):
a ;b ;c ;d ;e 。
(2)如果a是一种常见气体,试推断这五种物质(用化学式表示):
a ;b ;c ;d ;e 。
27.(6分)现有X、Y、Z三种短周期元素,原子序数依次增大,它们原子的最外层电子数之和为20,X、Y是同周期相邻元素,Y、Z是同主族相邻元素。写出它们的元素符号:X 、Y 、Z 。
26.(7分)有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl
(1)只由离子键构成的物质是________;(2)只由极性键构成的物质是________;
(3)只由非极性键构成的物质是____;(4)只由非金属元素组成的离子化合物是____;
(5)由极性键和非极性键构成的物质是______________;
(6)由离子键和极性键构成的物质是_____________;
(7)由离子键和非极性键构成的物质是________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com