
题目列表(包括答案和解析)
4.下列各组原子序数表示的两种元素,能形成AB2型离子化合物的是( )
A.12和17 B.13和16 C.11和17 D.6和8
3.M层有2个电子的元素A和L层有5个电子的元素B,组成稳定的化合物,该化合物的摩尔质量为( )
A.88g/mol B.40 g/mol C. 100 g/mol D. 72 g/mol
2.下列各组物质中都是由分子构成的化合物的是( )
A.CO2、NO2、NH4Cl B.HCl、NH3、CH4 C.NO、CO、CaO D.O2、N2、Cl2
1.下列燃料不属于化石燃料的是( w.w.^w.k.&s.5* )
A.煤 B.石油 C.天然气 D.水煤气
22.(10分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):

已知:a 常见双原子单质分子中,X分子含共价键最多。
b 甲分子中含10个电子,乙分子含有18个电子。
(1)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
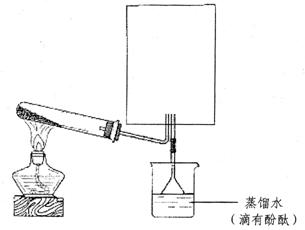
①在图中方框内绘出用烧瓶收集甲的仪器装置图。
②试管中的试剂是(填写化学式) 。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
(2)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是 。(磷的相对原子质量为31)
(3)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是 。
21.(14分)现有X、Y、Z、A、B、C、D几种元素:
①X、Y、Z是原子核外有3层电子的金属元素,原子半径X<Y<Z。
②A、B是非金属元素,它们可与氢化合形成气态氢化物H2A和HB。室温时,A的单质为淡黄色固体,B的单质为液态。
③C是元素周期表中氧化性最强的元素。
④D的单质是常温下呈液态的金属。利用上述已知条件请回答下列问题:
(1)Y在周期表中的位置是 ;H2A的结构式为 ;
(2)B 单质的颜色为 。
(3)用电子式表示化合物YB2的形成过程 。
(4)C单质与水反应的化学方程式为 。
(5)X单质与氢氧化钠溶液反应的离子方程式为 。
(6)A元素一种原子的质子数等于中子数,写出A的原子组成符号 。
(7)D单质的蒸气扩散到空气中会对人体产生危害,通常在洒落的D单质上覆盖硫磺进行处理,写出反应的化学方程式 。
20.(9分) 
(1)上表中的实线是元素周期表部分边界,请在表中用实线补全主族元素边界
(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物
写出其电子式 ,
(3)元素乙是第三周期金属元素中原子半径最小的元素,写出工业上制金属乙的化学方程式___________________
(4)化合物B是由甲元素和乙元素形成的化合物,将化合物A与化合物B等物质的量溶于水中,向其中滴加过量的2 mol·L-1氢氧化钠溶液,直至形成透明溶液。请根据实验现象出现的先后顺序,依次写出离子方程式______________________。
 18.(3分)(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
18.(3分)(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
19.(13分)元素X、Y、Z、W均为短周期元素,且原子序数依次增大。已知Y原子最外层电子数占核外电子总数的3/4,W-、Z+、X+半径逐渐减小,化合物XW常温下为气体,Z是本周期中除稀有气体元素外,原子半径最大的元素。据此回答下列问题:
(1)W在元素周期表中的位置是 ,实验室制取W单质的离子方程式为 。
(2)A、B均为由上述四种元素中的三种组成的强电解质,组成元素的原子数目比均为1:1:1。若为强碱,则A的电子式是 , B的化学式是 。
(3)C是由上述四种元素中的两种组成的一种含有非极性键的离子化合物,则C的名称为为 。
(4)用B在碱性条件下可以处理含CN-的工业废水,请将下列6种微粒:CN-、 、N2、OH-、B中阴离子、W的阴离子,分别填入下面对应的横线上,组成一个配平的离子方程式: + + = + + +
、N2、OH-、B中阴离子、W的阴离子,分别填入下面对应的横线上,组成一个配平的离子方程式: + + = + + + 
(5)X与Y形成的18电子分子与同样是18电子分子的H2S在水溶液中反应生成一种单质的化学方程式 ,可观察到的实验现象是
17.现有下列短周期元素性质的数据:下列关于表中11种元素的说法正确的是
|
元素符号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
?⑾ |
|
原子半径(10-10m) |
- |
0.37 |
0.74 |
0.75 |
0.77 |
0.82 |
0.99 |
1.10 |
1.52 |
1.60 |
1.86 |
|
最高或最 低化合价 |
0 |
+1 |
|
+5 |
+4 |
+3 |
+7 |
+5 |
+1 |
+2 |
+1 |
|
|
|
-2 |
-3 |
-4 |
|
-1 |
-3 |
|
|
|
A.11种元素中形成的非金属单质都有非极性共价键
B.②⑨处于同一周期,④⑧处于同一主族
C.11种元素中最高价氧化物对应的水化物,⑦号酸性最强
 D.⑥原子结构示意图为:
D.⑥原子结构示意图为:
16.在短周期元素组成的化合物中,若其原子个数比为1∶2,设两种元素的原子序数分别为a 和b,则下列对a和b可能关系的概括中,正确的是( )
①a+b=15 ②a=b+6 ③a=b-5 ④a+b=22
A. ①③ B. ①③④ C. ①②③④ D. ①②④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com