
题目列表(包括答案和解析)
4.下列元素中,最高正化合价数值最大的是
A.C B.S C.F D.Ne
3. 下列反应既属于氧化还原反应,又是吸热反应的是
A.锌粒与稀硫酸的反应
B.灼热的木炭与CO2的反应
C.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应
D. 甲烷在空气中燃烧的反应
2.医学研究证明,用放射性53135I治疗肿瘤可收到一定疗效下列有关53135I的叙述正确的是
A.53153I和Cl互为同位素
B.53135I是一种新发现的元素
C.53135I核内的中子数与核外电子数之差为29
D.53135I位于元素周期表中第4周期ⅦA族
1.物质的量相同的Mg2+、F-、H2O三种微粒,一定含有相同的
A.电子数 B.质子数 C.中子数 D.质量数
30.(1)1.00 L 1.00 mol·L-1 H2SO4溶液与2.00 L 1.00 mol·L-1 NaOH溶液完全反应,放出114.6 kJ的热量,由此可计算出中和热为______________kJ/mol。
(2)在25℃和101kPa的条件下,断开1 mol H-O键,吸收463 kJ能量;形成1 mol H-H键,放出436 kJ能量;形成1 mol O2 ,放出498 kJ能量, 试判断2 mol H2O分解成2 molH2和1 mol O2 时______________热______________ kJ。w.w.^w.k.&s.5*
29.不同元素的气态原子失去最外层的1个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。w.w.^w.k.&s.5*
 w.w.^w.k.&s.5*
w.w.^w.k.&s.5*
原子序数1至19号元素气态原子失去最外层的1个电子所需能量
(1)同主族内不同元素的E值变化的特点是:电子层数越大,________________________。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是______________。(填写编号,多选倒扣分)
①E(砷)>E(硒) ②E(砷)<E(硒) w.w.^w.k.&s.5* ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层的1个电子所需能量E值的范围:___________ kJ<E<_____________kJ。
(4)10号元素E值较大的原因是__________________________________。
28.现有原子序数依次递增的A、B、C三种元素,已知它们的最外层电子数之和等于氧原子最外层电子数,其核内质子数之和不超过18,它们均有两种氧化物:
A+O→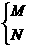 ,B+O→
,B+O→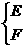 ,C+O→
,C+O→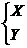 ,两种氧化物中氧元素质量分数:N>M,E>F,Y>X。M跟X化合,其生成物D与E反应时可能生成两种盐P或Q,其中Q可用来治疗胃酸过多的疾病。据此推断以上元素或化合物,回答下列问题:w.w.^w.k.&s.5*
,两种氧化物中氧元素质量分数:N>M,E>F,Y>X。M跟X化合,其生成物D与E反应时可能生成两种盐P或Q,其中Q可用来治疗胃酸过多的疾病。据此推断以上元素或化合物,回答下列问题:w.w.^w.k.&s.5*
(1)其中元素B位于周期表中 周期 族。
(2)画出A元素的原子结构示意图:__________________________________。
(3)写出F的化学式: F______________,写出E的结构式: E______________,
写出下列物质的电子式: N______________, X______________。
(4)Y是离子化合物,构成Y的阳离子与阴离子的离子个数比为______________。
(5)将标准状况下的2.24L E物质通入80mL 2mol/LNaOH溶液中,充分反应后,生成P和Q的物质的量之比为______________。
27.我国首创的海洋电池利用空气中的氧气与铝反应产生电流,电池总反应为4Al+3O2+6H2O=4Al(OH)3。据此回答:
(1)工作时,应将空气通入电池的 极。
(2)该电池负极电极反应式为: 。
(3)该电池正极材料可以从下列物质中选择_________(填编号w.w.^w.k.&s.5*)。
①铂网 ②镁网 ③石墨棒 ④塑料棒
(4)若在实验室模拟该电池的工作,电解质溶液可以从下列物质中选择________(填编号)。
①氯化钠溶液 ②纯水 ③盐酸 ④氢氧化钠溶液
(5)若导线上有1mol电子通过时,理论上会消耗Al________g。
26.下列各图为周期表的一部分。表中数字为原子序数,其中M为37的是( )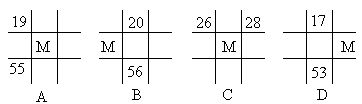
第Ⅱ卷(非选择题 共42w.w.^w.k.&s.5*分)
本卷为非选择题,请将答案填写在卷上相应的位置,共42分
25.设某元素原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A. 不能由此确定该元素的相对原子质量
B. 这种元素的相对原子质量为m+n
C. 若碳原子质量为wg,此原子的质量为(m+n)wgw.w.^w.k.&s.5*
D. 核内中子的总质量小于质子的总质量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com