
题目列表(包括答案和解析)
25.(6分)向NaOH和酚酞的混合液中滴入双氧水,红色消失,有的人认为是H2O2具有弱酸性,将NaOH溶液中和而使红色消失,有的人却认为是H2O2具有强氧化性,将有色物质氧化成无色物质而永久性褪色。
(1)请设计一个简单的实验证明谁的观点正确:___________________________________。
(2)含ClO- 的溶液和H2O2发生激烈反应 ,产生能量较高的氧分子,它立即转变为普通氧分子,向反应后的溶液中加入酸化的硝酸银溶液,有白色沉淀则ClO-与H2O2反应的离子方程式是: ,H2O2在反应中表现出________性
(填氧化或还原)
24.(10分)A、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的。试确定:
|
|
B |
|
|
A |
X |
C |
|
|
D |
|
(1)A、D的元素符号:A_______;D_______;
B的原子结构示意图______;C离子的结构示意图_______
A的气态氢化物的结构式______;B的气态氢化物的电子式_______
(2)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:_______________________。
(用化学式表示,下同)
(3)写出A、B、X气态氢化物的稳定性由强到弱的顺序:_______________________。
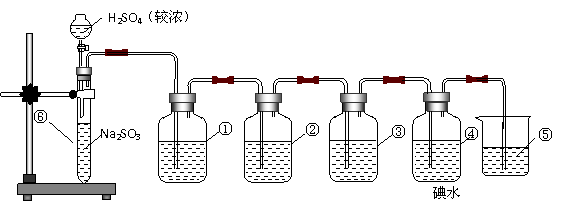
23.(11分)下图是实验室制SO2并验证SO2某些性质的装置图。试回答:
|
|
|
|
(1 ①中的实验现象为 ,有关化学方程式为 ;
(2) ②中的实验现象是 ,证明SO2有 性;
(3) ③中的实验现象是 ,证明SO2有 性;
(4) ④中的实验现象是 ,证明SO2有 性;
(5)装置⑤中反应的离子方程式为: 。
22.(8分)某溶液中可能存在下列离子中的一种或几种:CO32-、SO32-、SO42-、Br-
(1)当溶液中有大量H+存在时,溶液中不可能有较多的离子是 ;
(2)当溶液中有大量Ba2+存在时,溶液中不可能有较多的离子是 ;
(3)当溶液中有大量一价阳离子 存在时,以上四种离子都不可能大量存在 ;
(4)当溶液中通入Cl2时, 离子可被氧化。
21.(3分)在下列物质中:①碘单质②烧碱③NaCl④干冰⑤氯化氢⑥Na2O2。用序号填写下列空白:
(1)既含有离子键又含有非极性键的化合物是
(2)仅含有离子键的化合物是
(3) 仅含有共价键的单质是
20. 一定物质的量的SO2与NaOH反应,所得溶液中含Na2SO3与NaHSO3物质的量之比为3:5,则参加反应的SO2与NaOH物质的量之比为( )
A.3:5 B.1:2 C.11:8 D.8:11
第二卷(非选择题 共50分)
19. 有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子
数相同(选项中m、n均为正整数)。下列说法正确的是( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
18. 下列分离混合物试剂、方法正确的是( )
|
|
混合物(括号内为杂) |
分离提纯的试剂 |
分离提纯的方法 |
|
A |
CO2(SO2) |
饱和食盐水 |
洗气 |
|
B |
SO2(HCl) |
亚硫酸钠溶液 |
洗气 |
|
C |
CO2(CO) |
氧化铜粉末 |
气体通过赤热CuO |
|
D |
Na2SO3(Na2SO4) |
氯化钡溶液 |
过滤 |
17. 向盐酸中加入浓硫酸会有白雾产生,下列叙述中与此现象无关的是 ( )
A.浓硫酸具脱水性 B.浓硫酸具有吸水性
C.盐酸具有挥发性 D.气态物质的溶解度随温度的升高而降低
16. 在一定体积的18mol·L-1的浓硫酸中加入过量铜片并加热,被还原的硫酸为0.9mol,则浓硫酸的实际体积为 ( )
A.等于50 mL B.大于50 mL C.等于100 mL D.大于100 mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com