
题目列表(包括答案和解析)
2..对化学反应限度的叙述,错误的是 A.任何可逆反应都有一定的限度
B.化学反应达到限度时,正逆反应速率相等 C.化学反应的限度与时间的长短无关 D.化学反应的限度是不可改变的
1. 下列各组中属于同位素关系的是
A、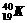 与
与 B、T2O与D2O C、
B、T2O与D2O C、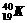 与
与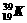 D、金刚石与石墨
D、金刚石与石墨
22. 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:
3A(g)+B(g)= xC(g)+2D(g)
经5min后,测得c(D)=0.5mol/L, 5min里C的反应速率是0.1mol/(L·min)。
求:(1)5min里,用B表示的反应速率; (2)X值。
2009-2010学年度第二学期宣中、广中高一年级期中联考
21. (9分)已知10℃时,某反应中各物质的物质的量随时间的变化关系如图所示(X、Y、Z均为气体),容器的容积为3L,反应过程中温度和容器的容积保持不变。试回答下列问题:
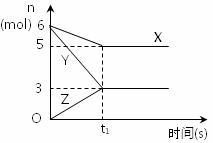 (1)该反应的化学方程式为
;
(1)该反应的化学方程式为
;
(2)若t1=10s,则这段时间内Y物质的平均反应速
率为 ;
(3)若该温度下其反应速率为v,温度每升高10℃,化学反应速率增大为原来的2倍,则温度升高至50℃时,其反应速率为 。(用含字母v表示)
20.(13分)下表是元素周期表的一部分, 针对表中的①-⑨种元素,填写下列空白:
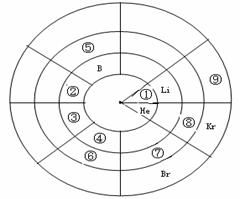 (1) 在这些元素中,化学性质最不活泼的是
,非金属性最强的元素是 ;(填元素符号)。
(1) 在这些元素中,化学性质最不活泼的是
,非金属性最强的元素是 ;(填元素符号)。
(2) 在最高价氧化物的水化物中,碱性最强的化合物的电子式是:_____________。
(3)用电子式表示⑥的氢化物的形成过程 ,该化合物属于 (填 “共价”或“离子”)化合物。
(4)④和⑨的单质加热时反应生成一种原子个数比为1:1的化合物X,其化学式为 ,该物质中含有的化学键的类型为 。(若含共价键,请写清极性键还是非极性键)
(5)表中能形成两性氢氧化物的元素是 (填元素符号),写出该元素的单质与⑨的最高价氧化物对应水化物反应的离子方程式 。
19.(8分)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)A中反应的离子方程式为____________________。
(2)B中Sn极的电极反应式为____________________,Sn极附近溶液的pH___________(填“增大”、“减小”或“不变”)。
(3)C中负极金属是________,总反应的化学方程式为_________________________。
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________。(用A、B、C表示)
18.(8分)用“>”或“<”回答下列问题:
(1)酸性: H2SiO3 H3PO4
(2)碱性:KOH Ca(OH)2
(3)氢化物稳定性:H2S H2O
(4)还原性:PH3 H2S
17.(6分)在原子序数1-18号的元素中:(用元素符号或化学式填空)
(1)与水反应最剧烈的金属是__________。 (2)与水反应最剧烈的非金属单质是_______。
(3)原子半径最小的元素形成的单质是___________。
(4)气态氢化物水溶液呈碱性的元素是________。
(5)最稳定气态氢化物的化学式是________。
(6)最高价氧化物对应水化物的酸性最强的物质是_____________
16.化学反应速率v和反应物浓度的关系可由实验方法测定的.化学反应H2+Cl2=2HCl的反应速率v=K[c(H2)]m·[c(Cl2)]n,式中的K为常数,m、n值可用下表中的数据确定出:
|
c(H2)mol·L-1 |
c(Cl2)(mol·L-1) |
v(mol·L-1·S-1) |
|
1.0 |
1.0 |
1.0k |
|
3.0 |
1.0 |
3.0k |
|
3.0 |
4.0 |
6.0k |
由此可推得m、n值正确的是( )
A. m=1, n=1 B. m=0.5, n=0.5 C. m=1, n=0.5 D. m=0.5, n=1
第Ⅱ卷 非选择题 (共52分)
15.在一定温度下,可逆反应A(g)+3B(g)  2C(g)达到平衡状态的标志是( )
2C(g)达到平衡状态的标志是( )
A.单位时间内生成n mol A,同时生成3n mol B
B.单位时间内生成C 2m mol,同时生成m mol A
C.反应速率v (A) ∶v (B )∶v (C)之比为1∶3∶2
D.A、B、C的分子数比为1∶3∶2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com