
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
26ЁЂ(1)
|
Ђк |
ЁЁ |
ЁЁ |
ЁЁ |
ЁЁ (III)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ |
|
Ђл |
ЁЁ |
ЁЁ |
ЁЁ |
|
|
Ђм |
ЁЁ |
ЁЁ |
ЁЁ |
(2)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3) Ип*ПМ*зЪ-дД+Эј

ФЕвЛжа2009-2010бЇФъЯТбЇЦкЦкжаПМЪд
ИпвЛбЇФъЛЏбЇПЦЪдЬт1ЬзОэ( ЙВ100 Зж)Ип*ПМ*зЪ-дД+Эј
25ЁЂ(1)ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ(2)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ
(3)ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(5)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁИп*ПМ*зЪ-дД+Эј
24ЁЂ(1)ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ(2)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(5)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
23ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
26ЁЂ(12Зж)ФГЬНОПаЁзщгУHNO3гыДѓРэЪЏЗДгІЙ§ГЬжажЪСПМѕаЁЕФЗНЗЈЃЌбаОПгАЯьЗДгІЫйТЪЕФвђЫиЁЃЫљгУHNO3ХЈЖШЮЊ1.00mol/LЁЂ2.00mol/LЃЌДѓРэЪЏгаЯИПХСЃКЭДжПХСЃСНжжЙцИёЃЌЪЕбщЮТЖШЮЊ25ЁцЁЂ35ЁцЃЌУПДЮЪЕбщHNO3ЕФгУСПЮЊ25.00mLЃЌДѓРэЪЏгУСПЮЊ10.00gЁЃ
(1)ЧыЭъГЩвдЯТЪЕбщЩшМЦБэЃЌВЂдкЪЕбщФПЕФвЛРИжаЬюПеЃК
|
ЪЕбщ БрКХ |
ЮТЖШ (Ёц) |
ДѓРэЪЏ ЙцИё |
HNO3ХЈЖШ(mol/L) |
ЪЕбщФПЕФ |
|
Ђй |
25 |
ДжПХСЃ |
2.00 |
(I)ЪЕбщЂйКЭЂкЬНОПХЈЖШЖдЗДгІЫйТЪЕФгАЯьЃЛ (II)ЪЕбщЂйКЭЂлЬНОПЮТЖШЖдЗДгІЫйТЪЕФгАЯьЃЛ (III)ЪЕбщЂйКЭЂмЬНОПЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЖдЗДгІЫйТЪЕФгАЯь |
|
Ђк |
ЁЁ |
ЁЁ |
ЁЁ |
|
|
Ђл |
ЁЁ |
ЁЁ |
ЁЁ |
|
|
Ђм |
ЁЁ |
ЁЁ |
ЁЁ |
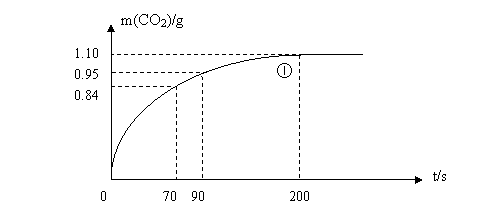
(2)ЪЕбщЂйжаCO2жЪСПЫцЪБМфБфЛЏЕФЙиЯЕМћЯТЭМЁЃМЦЫуЪЕбщЂйжа70s-90s
ЗЖЮЇФкгУHNO3БэЪОЕФЦНОљЗДгІЫйТЪЁЁЁЁЁЁЁЁЁЁЁЁ (КіТдШмвКЬхЛ§ЕФБфЛЏ)
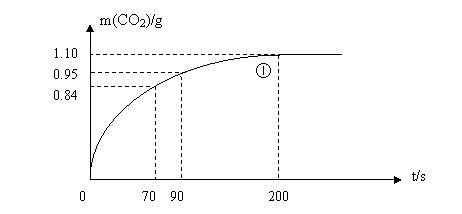

(3)ЧыдкЩЯЭМжаЛГіЪЕбщЂкЂлЂмжаCO2жЪСПЫцЪБМфБфЛЏЕФЙиЯЕЕФдЄЦкНсЙћЪОвтЭМЁЃ
|
 ФЕвЛжа2009-2010бЇФъЯТбЇЦкЦкжаПМЪд
ФЕвЛжа2009-2010бЇФъЯТбЇЦкЦкжаПМЪд
ИпвЛбЇФъЛЏбЇПЦ1ЬзОэ Д№ЬтПЈ( ЙВ100 Зж)
25ЁЂ(16Зж)a,b,c,d,eЪЧЖЬжмЦкдЊЫиЃЌжмЦкБэжаaгыbЃЌbгыcЯрСкЃЌcгыeЭЌжїзхЃЌaгыcЕФзюЭтВуЕчзгЪ§жЎБШЮЊ2ЃК3ЃЌbЕФзюЭтВуЕчзгЪ§БШcЕФзюЭтВуЕчзгЪ§ЩйвЛИіЃЌГЃМћЛЏКЯЮяd2c2гыЫЎЗДгІЩњГЩcЕФЕЅжЪЃЌЧвШмвКЪЙЗгЬЊШмвКБфКьЁЃ
(1)eЕФдЊЫиЗћКХЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)a,b,cЕФЧтЛЏЮяЮШЖЈадгЩЧПЕНШѕЕФЫГађЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)bЕФЧтЛЏЮяКЭbЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяЗДгІЩњГЩzЃЌ zЕФЛЏбЇЪНЮЊЁЁЁЁЁЁ
zжаЕФЛЏбЇМќРраЭЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁzЕФЛЏКЯЮяРраЭЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЙВМлЛЏКЯЮяЛђРызгЛЏКЯЮя)
(4)аДГіd2c2гыac2ЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(5)вЛЖЈСПЕФd2c2гыac2ЗДгІКѓЕФЙЬЬхЮяжЪЃЌЧЁКУгы1L 0.8mol/LHClЭъШЋЗДгІЃЌЩњГЩ0.25molЦјЬхЁЃЧыаДГіИУЙЬЬхЮяжЪЕФЛЏбЇЪНМАЦфЮяжЪЕФСПЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
24ЁЂ(12Зж)ЖЬжмЦкжїзхдЊЫиAЁЂBЁЂCЁЂDЕФдзгађЪ§вРДЮдіДѓЃЌЦфжаAЁЂCЭЌ
жїзхЃЌBЁЂCЁЂDЭЌжмЦкЃЌAдзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ3БЖЃЌBЪЧ
ЖЬжмЦкдЊЫижадзгАыОЖзюДѓЕФжїзхдЊЫиЁЃЪдЛиД№ЯТСаЮЪЬт(гУдЊЫиЗћКХЛиД№)ЃК
(1)AЕФдЊЫиЗћКХ ЁЁЁЁЁЁЁЁЁЁЃЛDЕФдзгНсЙЙЪОвтЭМЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)AЁЂBЁЂCШ§жждЊЫиаЮГЩЕФМђЕЅРызгЕФАыОЖгЩДѓЕНаЁЕФЫГађЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)AЁЂBЁЂCЁЂDаЮГЩЕФЛЏКЯЮяB2A2ЁЂCD2жаЃЌИїдзгЛђРызгзюЭтВуЖМТњзу8ЕчзгНсЙЙЕФЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)гУЕчзгЪНБэЪОB2AЕФаЮГЩЙ§ГЬЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(5)CA2гыDЕФЕЅжЪдкЫЎжаЗЂЩњбѕЛЏЛЙдЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЃ
23ЁЂ(4Зж)КНЬьММЪѕжаЪЙгУЕФЧтбѕШМСЯЕчГиОпгаИпФмЁЂЧсБуКЭВЛЮлШОЛЗОГЕШгХЕуЁЃ
ЧтбѕШМСЯЕчГигаЫсЪНКЭМюЪНСНжжЃЌЫќУЧЗХЕчЪБЕФзмЗДгІЪНЖМПЩБэЪОЮЊЃК
2H2+O2=2H2OЁЃМюЪНЧтбѕШМСЯЕчГиЕФЕчНтжЪЪЧМюЃЌЦфе§МЋЗДгІЪНЮЊЃК
O2+2H2O+4e-=40H-ЃЌИКМЋЗДгІЪНЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
22ЁЂМИжжЖЬжмЦкдЊЫиЕФжївЊЛЏКЯМлМАдзгАыОЖЪ§ОнМћЯТБэЃК
|
дЊЫиДњКХ |
L |
M |
Q |
R |
T |
|
жївЊЛЏКЯМл |
+2 |
+3 |
+6ЁЁ
-2 |
+7ЁЁЁЁ
-1 |
-2 |
|
дзгАыОЖ/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.074 |
ОнБэжааХЯЂХаЖЯЃЌЯТСагаЙиа№Ъіжае§ШЗЕФЪЧ(ЁЁ ) AЃЎLЁЂMЕФЕЅжЪЗжБ№гыЭЌХЈЖШЕФЯЁбЮЫсЗДгІЪБЃЌMЕФЕЅжЪЗДгІИќОчСв BЃЎMгыTаЮГЩЕФЛЏКЯЮяФмКЭЧПЫсЁЂЧПМюЗДгІ CЃЎLгыRСНдЊЫиаЮГЩЕФЛЏКЯЮяжаКЌгаЙВМлМќ DЃЎQЁЂTСНдЊЫиЕФЧтЛЏЮяШШЮШЖЈадБШНЯЃКQЕФЧтЛЏЮяДѓгкTЕФЧтЛЏЮя
21ЁЂвбжЊRn- +2RO32-+ 6H + =3R +3H2O(RЮЊЖЬжмЦкдЊЫи)ЃЌЯТСаХаЖЯе§ШЗЕФЪЧ( ЁЁ)
AЃЎВЛФмШЗЖЈRЕФзхађЪ§ЁЁЁЁ ЁЁЁЁBЃЎRO32-жаRдЊЫижЛФмБЛЛЙдВЛФмБЛбѕЛЏ
CЃЎRЕФзюИпМлЮЊ+4МлЁЁЁЁЁЁ ЁЁЁЁDЃЎRдЊЫиЪЧS
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com