
题目列表(包括答案和解析)
6.有关化学用语正确的是
A.Cl-的电子排布式:1s22s22p63s23p6
 B.乙醇的结构简式:C2H6O
B.乙醇的结构简式:C2H6O
C.硫离子的结构示意图:

D.四氯化碳的电子式:
5.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪种原子不能产生NMR现象
A.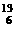 C B.
C B. N
C.
N
C. O D.
O D.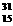 P
P
4、以下能级符号不正确的是( )
A. 3s B. 3p C . 3d D. 3f
3.在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.P轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
2.下列生活中的问题,不能用金属键理论知识解释的是( )
A.用铁制品做炊具 B.用金属铝制成导线
C. 用铂金做首饰 D.铁易生锈
1、一个电子排布为1s22s22p63s23p1的元素最可能的价态是( )
A. +1 B. +2 C. +3 D. -1
23.将等物质的量的氢气和碘蒸气放入2L密闭容器中进行反应:
H2(g)+I2(g)  2HI(g)(正反应放热), 反应经过5分钟测得碘化氢的为0.5mol,碘蒸气为0.25mol。请填写以下的空白:
(1)vHI=
;vH2= ;氢气的起始浓度= 。
(2)若上述反应达到平衡时,则平衡浓度HI、I2、H2的关系是 。
2HI(g)(正反应放热), 反应经过5分钟测得碘化氢的为0.5mol,碘蒸气为0.25mol。请填写以下的空白:
(1)vHI=
;vH2= ;氢气的起始浓度= 。
(2)若上述反应达到平衡时,则平衡浓度HI、I2、H2的关系是 。
 (填“相等”、“2︰1︰1”或“均为恒量”)
24.如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气
(填“相等”、“2︰1︰1”或“均为恒量”)
24.如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气
(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略。
将封闭有甲烷和氯气的混和气体的装置放置在有光亮的地方,
让混和气体缓慢的反应一段时间。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写
出化学方程式: 。写出甲烷
的结构式:__________。
(2)经过几个小时的反应后,U型管右端的玻璃管中水柱变化是 。
A.升高 B.降低 C.不变 D.无法确定
(3)U型管左端的气柱变化是 。
A.体积增大 B.体积减小 C.消失 D.不变
22.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
|
实验步骤 |
实验现象 |
|
①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
|
②向新制得的Na2S溶液中满加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
③将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体. |
|
④将镁条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
|
⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
|
⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器:① ,② ,烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号)(各1分)
|
实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
|
实验现象(填A-F) |
|
|
|
|
|
|
步骤①的化学方程式: ,
步骤⑥的离子方程式 ,
此实验的结论: 。
21.短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称: A B D
(2)E在周期表中的位置: __________________________________
(3)F离子结构示意图: __________________
(4)A、B组成的最简单化合物的名称是___________
(5)用电子式表示BC2的形成过程
(6)C单质与D单质在常温下反应的产物的电子式_______________________
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为______________,将W溶于水的化学方程式__________________________________,W的用途有______________
(填一种)
(8)能说明E的非金属性比F的非金属性____(填“强”或“弱”)的事实是:
___________________________________________________________ (举一例)。
20.下列说法正确的是
A.组成元素相同、式量相同、结构不同的有机物都互为同分异构体
B.具有同一通式、分子组成上相差若干个CH2原子团的物质一定属于同系物
C.化学式相同而结构不同的有机物一定互为同分异构体
D.只要化学式量相同就一定属于同分异构体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com