
题目列表(包括答案和解析)
17.下列属于纯净物的是
A. 蒸溜水 B. 石油 C. 碘酒 D. 空气
13.(8分)为了测定某赤铁矿石中氧化铁的质量分数,取矿石样品40g,加入盐酸,恰好完全反应时,共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g(矿石中的杂质既不溶于水也不与盐酸反应)。计算:
(1)赤铁矿石中氧化铁的质量分数;
(2)盐酸的溶质质量分数。
威海市二○一○年年初中升学考试
12.(14分)有三种失去标签的溶质质量分数分别为15%、l0%和5%的盐酸溶液。限定你选择下列仪器和药品,设计两种不局的实验方案,辨别出最浓的和最稀的盐酸溶液。
实验仪器:精密温度计、剪刀、镊子、量筒、秒表、烧杯、大试管、胶头滴管。
药 品:镁条
提 示:①镁条和盐酸反应速度很快,通过观察放出气泡速度很难准确判断盐酸浓度的大小,所以不建议用这种方法辨别之。②当你设计一种方案时,不必用到所有的仪器。③在描述每种实验方案时,要求说明:观察或测定何种变量、需要控制的条件、选用的仪器、实验步骤及结果与推论。
(1)实验知识和技能准备:
用量筒量取一定体积的液体时,正确的操作方法是___________________________________________
______________________________________________________________________________________________________________________________________________________________________________________
向试管中加入块状固体药品的方法是_______________________________________________________
___________________________________________________________________________________________
(2)把你设计的实验方案依次填写在下表中.
实验方案一:
|
你观察或 测定的量 |
需要控制 的实验条件 |
选用的 仪器 |
实验步骤 |
结果与推论 |
|
|
|
|
|
|
实验方案二:
|
你观察或 测定的量 |
需要控制 的实验条件 |
选用的 仪器 |
实验步骤 |
结果与推论 |
|
|
|
|
|
|
(3)为了排除实验过程中偶然因素的干扰,保证实验结果的可靠性,你认为还应该如何完善你的实验方案?
___________________________________________________________________________________________
11.(5分)燃烧的“利”与“弊”
火就是化学上所说的燃烧。根据你对燃烧反应的理解,若以“燃烧的利与弊”做为论题,你的观点是_______________________________,请你列举有力的证据论证你的观点。
要求:①论据简洁、论证充分。②同一论据只需举出一个事例说明即可。③字数在150字以内。
(25×6=150)
10.(7分)应用广泛的金属
没有金属,生活是难以想象的。请你根据所学知识回答下列问题:
(1)只要观察一下你的周围,你就能理解金属是多么有用。在一百余种元素中,金属元素的种类比非金属元素的种类________。由于金属具有特殊的组成和结构,决定了金属具有优良的物理性能。你认为金属比较重要的两种物理性质是____________________________。
现代社会以各种金属为支撑,其中用量最大、应用最广泛的金属是_________。地壳中含量最丰富的金属是__________。
(2)尽管金属有非常优良的物理性质,但应用金属经常遇到的问题是大多数金属化学性质活泼,易与其它物质发生反应。例如,大多数金属暴露在空气中易被腐蚀,这是因为金属易与氧气发生反应,该反应的实质是_________反应。从金属的原子结构看,你认为金属易与其它物质发生反应的根本原因是______________________________________________。
(3)我国早在春秋战国时期就开始炼铁、应用金属铁。请你用化学方程式表示用一氧化碳还原氧化铁的化学反应原理______________________________________。
9.(12分)地球“发烧”了
材料l.空气的成分
空气是多种气体的混合物。空气的成分可分为恒定成分和易变成分两类。恒定成分是指在空气中含量大,在任何地方含量几乎不变,包括78.06%氮气、20.94%氧气、0.94%氩等稀有气体,合计约占99.94%。易变成分是指在空气中含量很少,但因季节、地域等自然因素和人类的活动而引起相对含量的较大变化,甚至某些成分急剧增加或减少。下表中列出了大气中几种易变成分:
|
易变成分(浓度cm3/m3) |
变化的原因 |
|
二氧化碳 约300(约占空气的0.03%) |
|
|
水蒸气 约290(约占空气的0.03%) |
|
|
甲烷 约1.0-1.2 t |
天然气泄漏 |
|
氮的氧化物约0.52 |
化石燃料的燃烧 |
|
臭氧 0.01-0.04 |
含氟化合物的使用 |
|
硫的化合物:二氧化硫、硫化氢等 |
化石燃料的燃烧等 |
|
一氧化碳 |
汽车尾气等 |
|
合计: 0.06% |
|
材料2.自然界中碳循环
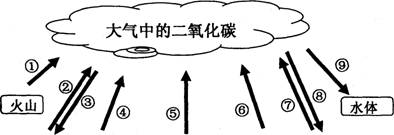



自然界中碳循环
试回答下列问题:
(1)从地球上动植物生命活动所需要的物质角度看,为什么空气如此重要?
(答出3条即可)
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(2)大气中多余的二氧化碳从何而来?
从上述材料可以看出,人类赖以生存的大气,正遭受空前严重的破坏。二氧化碳作为一种主要的温室性气体,含量增加导致气候变暖、地球“发烧”、灾害频发,成为当前威胁人类生存发展最严重的问题。分析材料2,你认为导致大气中二氧化碳含量增加的直接原因是(写出两条即可)_____________________
__________________________________________________________________________________________
在②中,以石灰石为例,分解反应的化学方程式为__________________________________。
在⑧中,消耗二氧化碳的过程叫做___________________。在⑨中,消耗二氧化碳反应的化学方程式为__________________________________。在④中,以天然气为例,燃烧反应的化学方程式为___________
__________________________________。
(3)如何除去大气中多余的二氧化碳?
据统计,大气中每年新增CO2约为l85-242亿吨,而其综合利用还不足l亿吨/年,仅靠碳的自然循环来平衡大气中二氧化碳已不可能。为了降低大气中二氧化碳的含量,化学家们正想尽办法用化学反应的手段使二氧化碳“变废为宝”。
①火电厂用碱液吸收产生的二氧化碳,获得化工产品碳酸钠。该反应的化学方程式为______________
___________________________。
②日本科学家研制成功一种新型催化剂,在常压、300℃条件下,CO2和H 2反应生成甲烷和水。该反应的化学方程式为_________________________________。
③用三甲基膦做催化剂,在高压、极低温度条件下,CO2和H 2可以高效合成甲酸(HCOOH),并实现了工业化生产。该反应的化学方程式为______________________________________________。
8.(13分)化学物质的多样性
世界是物质的,物质都是由化学元素组成的。到目前为止,已经发现自然界中存在的和实验室合成的物质超过三千万种,并且化学家还在以每年近百万种的速度继续发现更多的新物质。请你运用所学的知识回答下列问题。
(1) 在下表空白处填上适当的内容:
|
物质名称 |
物质组成 (用化学式表示) |
构成物质的微粒 (用符号表示) |
物质中各元素的质量比 |
|
氧气 |
O2 |
|
|
|
臭氧 |
O3 |
|
|
|
过氧化氢 |
|
|
mH:mO=1:l6 |
|
铜 |
Cu |
|
|
|
熟石灰 |
Ca(OH)2 |
|
|
|
|
|
Na+、CO32- |
mNa:mC:mO=23:6:24 |
|
蔗糖 |
|
|
mC:mH:mO=72:11:88 |
|
食盐水 |
|
|
|
(2) 由于物质的多样性,化学上通常用分类的方法认识物质。请你根据物质的组成,把(1)中8种物质分类,要求用框图的形式表示,层次分明。
(3)你认为造成物质多样性的原因有哪些?请选择(1)中物质说明(答三种即可):
原因① ,举例: ;
原因② ,举例: ;
原因③ ,举例: 。
7.下列关于溶液的说法中,不正确的是
A.溶液中各部分性质相同,是一种高级混合物
B.氢氧化钠溶液能导电,是因为溶液中含有自由移动的离子
C.接近饱和的硝酸钾溶液,通过蒸发溶剂或加溶质的方法都可以达到饱和状态
D.20℃,氯化钠的溶解度为36g,则20℃时100g氯化钠饱和溶液中含有氯化钠36g
绝密★启用前
威海市二○一○年六年初中升学考试
化 学
第Ⅱ卷(非选择题共59分)
6.下列鉴别物质的方法错误的是
A.用闻气味方法鉴别:NH3和O2
B.用酚酞试液鉴别:稀盐酸和氯化钠溶液
C.用沉淀法鉴别:Na2SO4溶液和NaNO3溶液
D.用燃烧法鉴别:H2和CO
5.2010年上海世博会的主题是“城市,让生活更美好”。开发使用新能源,是解决城市大气污染问题的根本途径。下列与新能源有关的说法中,不正确的是
A.研制、使用氢燃料电池汽车,能真正实现“零排放”,是解决汽车尾气污染的有效措施
B.晶体硅不仅是电子和信息工业的基础材料,也是研制太阳能电池的基础材料
C.核能不属于清洁能源
D.风能、水能、地热能均属于清洁能源
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com