
题目列表(包括答案和解析)
5.某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为( )
A.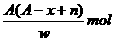 B.
B.
C. D.
D.
4.一定条件下,可逆反应2A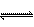 B+3C,在下列四种状态中处于平衡的是( )
B+3C,在下列四种状态中处于平衡的是( )
正反应速率 逆反应速率
A、ν(A)=2mol/(L·min) ν(B)=2mol/(L·min)
B、ν(A)=2mol/(L·min) ν(C)=2mol/(L·min)
C、ν(A)=1mol/(L·min) ν(B)=2mol/(L·min)
D、ν(A)=1mol/(L·min) ν(C)=1.5mol/(L·min)
3.某元素形成气态氢化物为HnR,其最高价氧化物水化物的分子式中有m个氧原子,则其最高价氧化物水化物的化学式为: ( )
A、H2m-8+nROm B、H2n-8+mROm C、H2ROm D、H2mROm
2.有关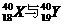 的说法正确的是 ( )
的说法正确的是 ( )
A、互为同位素 B、电子层数相等
C、单质是双原子分子 D、质量数相等
1.下列反应既是氧化还原反应,又是吸热反应的是 ( )
A、锌粒与稀硫酸的反应 B、灼热的木炭与CO2的反应
C、甲烷在氧气中的燃烧反应 D、Ba(OH)2·8H2O与NH4Cl的反应
31.(6分)利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。试计算:
(1)有多少个电子通过了导线。www.k*s*5*
(2)原稀硫酸溶液的物质的量浓度。
30.(6分)t℃时,将3molA和1molB气体通入容积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol·L-1。请计算:
xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol·L-1。请计算:
(1)从反应开始到平衡状态,生成C的平均反应速率;
(2)x的值;
29.(16分)动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
|
实验步骤 |
实验现象 |
|
① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
|
② 向新制得的Na2S溶液中滴加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
|
③ 将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体 |
|
④ 将镁条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
|
⑤ 将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
|
⑥ 向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉淀。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,
NaOH溶液,酚酞溶液等。
仪器和用品:① ,② ,③ ,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容: (填写与实验步骤对应的实验现象的编号和①②的化学方程式)
|
实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
|
实验现象(填A~F) |
|
|
|
|
|
|
① ,② ,
(4)此实验的结论:金属性比较: ,
非金属比较: 。
28.(8分)(1)右图是等质量的Na2CO3、NaHCO3粉末分别与足量的盐酸发生反应时的情景,产生CO2气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B两试管中消耗的盐酸的质量之比为__________。
 实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)


(a) (b)
(2)若Na2CO3 (aq) + HCl(aq) == NaHCO3(aq) + NaCl(aq) △H 1
NaHCO3(aq) + HCl(aq) == NaCl(aq) + H2CO3(aq) △H2
H2CO3(aq) == H2O(l) + CO2(g) △H 3
注:aq- 表示溶液中、 l- 表示液体、 g- 表示气体
试根据上述两组实验现象分别可得出的与△ H1、△ H2、△ H3有关的不等式为: _____ ________、________ ________。
27.(8分)下图中各物质均由短周期元素组成,其中只有D、F、G为单质,A为淡黄色固体,B为常见的无色液体,一定条件下D、G和海水为原料可制成海洋电池。
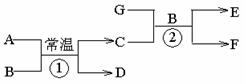
按要求填空:
(1)写出电子式A _________ B__________
(2)写出化学方程式①_ _ _______
②__ ________
(3)写出D、G和海水制成海洋电池的负极反应式_ ___。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com