
题目列表(包括答案和解析)
15.100 mL 6 mol·L-1 H2SO4 跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.碳酸钠固体  硝酸钠 C.硫酸钾固体 D.醋酸钠固体
硝酸钠 C.硫酸钾固体 D.醋酸钠固体
14.一定温度下反应N2(g)+3H2(g)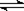 2NH3(g)达到化学平衡状态的标志是( )
2NH3(g)达到化学平衡状态的标志是( )
A.N2、H2和NH3的物质的量分数不再改变
 c(N2)∶c(H2)∶c(NH3)=1∶3∶2
c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C.N2与H2的物质的量之和是NH3物质的量的2倍
D.单位时间里每增加1molN2,同时减少2molNH3
13.将锌片和铜片用导线连接后放入稀硫酸溶液中发生原电池反应,下列叙述正确的是( )
A.负极附近的SO42-
浓度逐渐减小
 正极有O2逸出
正极有O2逸出
C.电子通过导线由铜片流向锌片 D.铜片k@s^5*u上有H2逸出
12.已知空气-锌电池的电极反应为:
锌片:Zn+2OH――2e-=ZnO+H2O;碳棒:O2+2H2O+4e- =4OH- ,据此判断,锌片是( )
A.正极,被还原
 正极,被氧化
正极,被氧化
C.负极,被还原 D.负极,被氧化
11.普通干电池负极的电极反应式是( )
A.Zn-2e-=Zn2+
 Zn2++2e-=Zn
Zn2++2e-=Zn
C.4OH--4e- =O2↑+2H2O D.2H++2e- =H2↑
10.元素周期表是一座开放的“元素大厦”,元素大厦尚未客满。若发现119号元素,请您在元素大厦中安排好它的“房间”
A.第七周期第0族  第六周期ⅡA族
第六周期ⅡA族
C.第八周期第ⅠA族 D.第七周期第ⅦA族
9.下列变化是因原电池反应而引起的是( )
A.在空气中金属铝表面迅速氧化形成保护膜
 常温下,铁被浓硫酸“钝化”形成保护膜
常温下,铁被浓硫酸“钝化”形成保护膜
C.在潮湿的空气中钢铁易生锈
D.在潮湿的空气中过氧化钠易变质
8.把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )
A.盐酸的浓度
 铝条的表面积
铝条的表面积
C.溶液的温度 D.加少量Na2SO4
7.下列反应既属于氧化还原反应,又是吸热反应的是( )
A.锌粒与稀硫酸的反应
 灼热的木炭与CO2的反应
灼热的木炭与CO2的反应
C.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 D.甲烷在空气中燃烧的反应
6.下列叙述正确的是( )
A.P4和NO2都是共价化合物
 CCl4和NH4Cl都是以共价键结合的分子
CCl4和NH4Cl都是以共价键结合的分子
C.在CaO和SiO2晶体中,都不存在单个小分子
D. 甲烷的结构式:  ,是对称的平面结构
,是对称的平面结构
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com