
题目列表(包括答案和解析)
3.下列有关电池的说法不正确的是
A.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
B.甲醇燃料电池可把化学能转化为电能
C.锂电池是一种二次电池
D.锌锰干电池中,锌电极是负极
2. 我国稀土资源丰富。下列有关稀土元素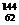 Sm与
Sm与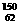 Sm的说法正确的是
Sm的说法正确的是
A.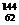 Sm与
Sm与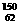 Sm互为同位素
Sm互为同位素
B.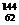 Sm与
Sm与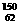 Sm的质量数相同
Sm的质量数相同
C.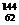 Sm与
Sm与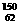 Sm是同一种核素
Sm是同一种核素
D.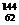 Sm与
Sm与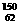 Sm的核外电子数和中子数均为62
Sm的核外电子数和中子数均为62
1. 下列说法中,错误的是
A.人类目前直接利用的能量大部分是由化学反应产生的
B.煤、石油、天然气是当今世界最重要的三种化石燃料
C.我国目前最主要的能源是煤炭
D.人体运动所消耗的能量与化学反应无关
22.(14分)某研究性学习小组用HNO3与大理石反应过程中质量减小的方法,探究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响。 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
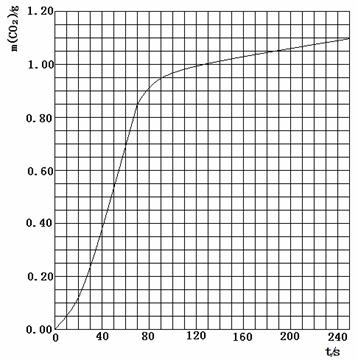
(2)实验①中CO2质量随时间变化的关系见下图:
依据反应方程式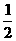 CaCO3+HNO3=
CaCO3+HNO3=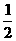 Ca(NO3)2+
Ca(NO3)2+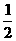 CO2↑+
CO2↑+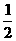 H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
21.(6分)已知化学能与其他形式的能可以相互转化。填写下表的空白:
|
化学反应方程式(例子) |
能量转化形式 |
|
① |
由化学能转化为热能 |
②Pb+PbO2+2H2SO4 2PbSO4+2H2O 2PbSO4+2H2O |
|
③CaCO3
 CaO+CO2↑ CaO+CO2↑ |
|
20.(7分)如图为原电池装置示意图:
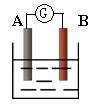
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A电极名称为 ,写出正极的电极反应式 。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则作铜片为 极(填正或负),写出电极反应式:正极 ,负极 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的 极(填正或负),该电池的总反应为: 。
19.(7分)如右图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题:
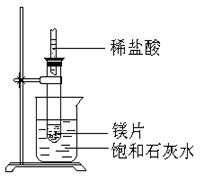
(1)实验中观察到的现象是 。
(2)产生该现象的原因 。
(3)写出有关反应的离子反应方程式 。
(4)有此推知,MgCl2溶液和H2的总能量 填(“大于”“小于”或“等于”)镁片和盐酸的总能量。
18.(6分)A、B、C、D、E、F、G都是由短周期元素构成的粒子,它们都有10个电子,结构特点如下表:
|
粒子代号 |
A |
B |
C |
D |
E |
F |
G |
|
原子核个数 |
单核 |
单核 |
双核 |
四核 |
单核 |
五核 |
五核 |
|
电荷数 |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
请填写下列空白:
(1)A粒子的结构示意图为 、D粒子的电子式为 、G粒子的化学式为 ;
(2)BC和EC2的碱性强弱为BC EC2(填:>、<或=);
(3)加热条件下,F与C在溶液中反应的离子方程式为 。
17.(12分)下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
|
① |
② |
③ |
|
|
3 |
④ |
⑤ |
⑥ |
⑦ |
|
|
⑧ |
⑨ |
|
4 |
⑩ |
|
|
|
|
|
|
|
(1)在①-⑩元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 。
(2)在①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的是 。写出在水溶液中三者之间相互反应的离子方程式: , , 。
16.C、CH4、CO、C2H5OH是常用的燃料,它们每1 mol 分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、890.3kJ、110.5kJ、1366.8kJ。相同质量的这4种燃料,完全燃烧时放出热量最多的是( )
A. C  CH4 C.CO D. C2H5OH
CH4 C.CO D. C2H5OH
第Ⅱ卷(非选择题,共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com