
题目列表(包括答案和解析)
22.(12分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
|
时间/min |
1 |
2 |
3 |
4 |
5 |
|
氢气体积/mL |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0-1、1-2、2-3、3-4、4-5 min)反应速率最大________,原因是________________________________________。
(2)哪一段时段的反应速率最小________,原因是________________________________。
(3)求2-3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)________________________________________。
 (4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)________。
21.(9分)利用反应“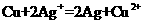 ”设计一个原电池(正极
”设计一个原电池(正极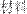 用碳棒)。
用碳棒)。
装置图:
回答下列问题:
(1)该电池的负极 是________,发生________反应(填“氧化”或“还原”),电极反应为:______________________________电解质溶液是________;
是________,发生________反应(填“氧化”或“还原”),电极反应为:______________________________电解质溶液是________;
(2)正极上出现的现象是________________________________;
(3)若导线上转移电子1 mol,则生成银________g。
20.(8分)(1)能源是当今社会发展的三大支柱之一。天然气是一种高效、低耗、污染小的清洁能源,主要成分为甲烷,甲烷燃烧的化学方程式为:__________________________准状况下,11.2L甲烷燃烧时,转移电子的物质的量为________mol,在如左下图构想的物质循环中太阳能最终转化为________能。
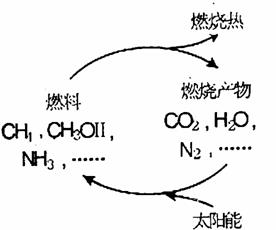
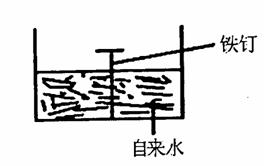
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀的主要原因,某同学按右上图进行钢铁腐蚀的模拟,则负极的电极反应式为________________________,正极的电极反应为________________________。
19.(8分)短周期元素A、B、C、D、E原子序数依次增大,含C元素的物质焰色反应为黄色,A、C位于同一主族,B的最外层电子数是次外层的3倍,D的最外层电子数是B最外层电子数的一半,B、C的最外层电子数之和与E的最外层电子数相等。请回答下列问题:
(1)E元素周期表中的位置是________。
(2)D单质与A、B、C三种元素组成的化合物的水溶液反应,其反应的离子方程式为________________________________________。
(3)0.25 mol A单质与足量的E单质反应,生成气体的体积(标准状况)为________。
(4)实验室欲检验CE盐溶液中所含的阴离子,操作方法和现象为:取少量的CE溶液于试管中,向其中滴加________________________,则证明溶液中有该阴离子。
18.(12分)元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。
|
A |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
D |
|
F |
|
|
|||||||
|
G |
|
Q |
|
|
M |
R |
|
||||||||||
|
N |
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
(1)表中T的元素符号为________,金属性最强的元素是________(填元素符号)。
(2)元素的非金属性:M________R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是________。
(4)F、G两元素形成的淡黄色固体物质的电子式为________________,该物质含有的化学键的类型是________________。
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径电大到小的顺序是________________________(填离子符号)。
(6)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为________________________________。
17.X、Y、Z是同周期的三种元素,已知其元素的非金属性:X>Y>Z。则下列说法正确的是 ( )
A.原子半径:X>Y>Z
B.原子序数:Z>Y>X
C.气态氢化物稳定性:X<Y<Z
D.最高价氧化物对应的水化物的酸性由强到弱的顺序是:X>Y>Z
16.下列各图中,表示正反应是吸热反应的图是 ( )

15.将4 mol A气体和2 mol B气体置于2 L的密闭容器中,混合后发生如下反应:2A(g) + B(g) = 2C(g)。若经2 s后测得C的浓度为0.6 mol/L,下列说法正确的是 ( )
A.用物质A表示的反应速率为0.6 mol/(L·s)
B.用物质B表示的反应速率为0.3 mol/(L·s)
C.2 s时物质A的转化率为30%
D.2 s时物质B的浓度为0.3 mol/L
14.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是
(m、n均为正整数) ( )
A.若R(OH)n为强碱,则W(OH)n+1也为强碱
B.若HnXOm强酸,则Y是活泼的非金属元素
C.若Y的最低化合价为-2,则Z的最高正化合价为+7
D.若X的最高正化合价为+5,则五种元素都是非金属元素
13.锌粒和盐酸反应一段时间后,反应速率减慢。此时加热或加入浓盐酸,反应速率明显加快。上述实验中影响化学反应速率的因素有: ( )
①温度 ②固体的表面积 ③反应物的状态 ④溶液的浓度 ⑤催化剂
A.①④ B。①③ C②④ D.①②③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com