
题目列表(包括答案和解析)
24.有1g液态烃完全燃烧后,得1.69LCO2(标况下),该物质的蒸气对空气的相对密度为3.655倍。求:
(1)该烃化合物的分子式;(写出计算过程)
(2)根据下列实验现象确定结构简式:
①它不能使溴水褪色但能使酸性KMnO4溶液褪色。
②它能发生硝化反应,当引入一个硝基时只能得到一种硝基化合物。
写出该烃及同类物质同分异构体的结构简式。
22.关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:
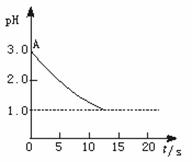 观点一是:“理论派”认为电解氯化铜溶液后
观点一是:“理论派”认为电解氯化铜溶液后
溶液的pH升高。
观点二是:“实验派”经过反复、多次、精确
的实验测定,证明电解氯化铜溶液时pH的变化
如图曲线的关系。 请回答下列问题:
(1)电解前氯化铜溶液的pH处在A点位置的
原因是 (用离子方程式说明)。 pH与时间关系图
(2)“理论派”所持观点的理论依据是 。
(3)你持何种观点? (填“理论派”或“实验派”)
理由是 (从化学原理加以简述)。
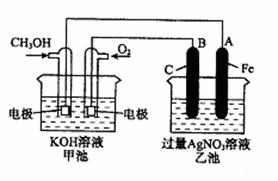 23.下图是一个化学过程的示意图,回答下列问题:
23.下图是一个化学过程的示意图,回答下列问题:
(1)甲电池是 装置,
乙池是 装置。
(2)通入CH3OH的电极名称
是 ,B电极的名称是 ;
(3)写出甲池中的电极反应式
,
;
(4)乙池中反应的化学方程式为 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)(Fe:56 Ag:108)
21.如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极.若A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1,合闭K2、K3通直流电,回答下列问题:
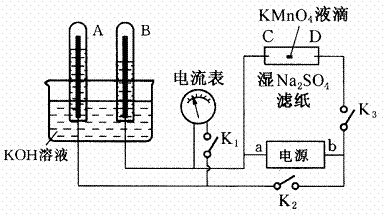
①判断电源的正、负极:a为________极,b为________极。
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象 。
③写出电极反应式:A极 ,
C极 。
④若电解一段时间后,A、B中均有气体包围电极.此时切断K2、K3,合闭K1,则电流表的指针是否移动(填是或否) ________。
说明理由 。
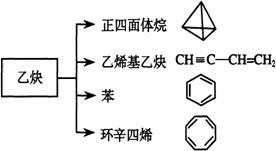
20、乙炔是一种重要的有机化工原料,以乙炔
为原料在不同的反应条件下可以转化成以下化
合物。完成下列各题:
(1)正四面体烷的分子式为 ,其中
C原子的杂化方式为 ,其二氯取代产物有 种
(2)关于乙烯基乙炔分子的说法错误的是:
a 能使酸性KMnO4溶液褪色
b 1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
c 生成乙烯基乙炔分子的反应属于取代反应
d 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
e 该分子中所有原子一定在同一平面内
(3)环辛四烯中C原子采用的杂化方式为 ,写出与它互为同分异构体且属于芳香烃的分子的结构简式:
(4)写出与苯互为同系物且一氯代物有三种的物质的结构简式(举两例):
、
19. 从石油中可分离出一种称为金刚烷的烃,它的结构与金刚石有类似之处,故而得名.图示为此烃的碳原子骨架.试填写下列空白:
从石油中可分离出一种称为金刚烷的烃,它的结构与金刚石有类似之处,故而得名.图示为此烃的碳原子骨架.试填写下列空白:
(1)此烃的化学式为________,
(2)它的分子内,连有2个氢原子的碳原子数是________,
(3)分子内由C原子构成的最小的环上有________个C原子,
这种环有________个.
(4)分子中C-C键的夹角为________.
18.某高分子材料的结构为
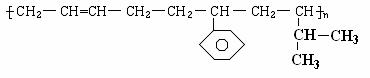
则其对应的单体有 , , 。
其名称依次为 , , 。
17.卤代烃在碱性水溶液中能发生水解反应,如:

请以CH3CH2OH为原料合成HOCH2CH2OH(反应条件和其它原料可以任选),写出合成过程中的各步反应的化学方程式(注明反应条件),并注明各有机反应的类型。
①
②
③
16.根据题干要求书写下列有关反应的方程式:
(1)由丙烯、HCl制备2-氯丙烷
(2)2-丁烯聚合成聚2-丁烯
(3)由甲苯制备TNT
(4)工业利用乙烯制乙醇
(5)3,3-二甲基-1-丁炔与足量氢气反应
15.在烃分子中去掉两个氢原子形成一个双键是吸热反应,大约需要17kJ·mol-1~125 kJ·mol-1的热量,但1,3-环已二烯失去两个氢原子变成苯是放热反应,ΔH= -23. 4 kJ·mol-1,以上事实表明( )
A. 1,3-环已二烯加氢是吸热反应 B.苯加氢生成环已烷是吸热反应
C. 1,3-环已二烯比苯稳定 D.苯比1,3-环已二烯稳定
14.C8H18经多步裂化,最后完全转化为C4H8、C3H6、C2H4、C2H6、CH4五种气体的混合物。该混合物的平均相对分子质量可能是( )
A.28 B.30 C.38 D.40
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com