
题目列表(包括答案和解析)
6. 具有下列条件的微粒中,其元素的非金属性最强的是
A.原子结构示意图为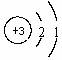 B.离子结构示意图为
B.离子结构示意图为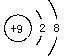
C.原子质量数为24,中子数为12 D.元素正、负化合价绝对值相同
5. 有四种物质:①四氯化碳 ②白磷 ③甲烷 ④石墨,其中分子具有正四面体结构的是
A、①②③ B、①③④ C、①② D、②③
4. 在盛有稀H2SO4的烧杯中放入用导线连接锌片和铜片,下列叙述正确的是
A、正极附近的SO42―离子浓度逐渐增大 B、电子通过导线由铜片流向锌片 C、正极有O2逸出 D、铜片上有H2逸出
3. 下列电子式书写错误的是
A.甲基 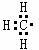 B.NH4+
B.NH4+ 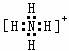 C.CO2
C.CO2  D.H-
D.H-
2. 下列离子化合物中阳离子半径和阴离子半径之比最大的是
A. LiI B.NaBr C.KCl D.CsF
1.下列有关化学键与晶体结构说法正确的是
A、两种元素组成的分子中一定只有极性键
B、离子化合物的熔点一定比共价化合物的高
C、非金属元素组成的化合物一定是共价化合物
D、含有阴离子的化合物一定含有阳离子
工业上用电解熔融氧化铝的方法制取金属铝。
(1)请写出反应的化学方程式
(2)现预冶炼270吨 Al,需要多少吨氧化铝?
24. (6分)下列事实中,什么因素影响化学反应速率?
(1)熔化的氯酸钾放出气泡很慢,撒入二氧化锰,产生气体很快 。
(2)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同 ,
(3)夏天的食物易霉变,冬天就不易发生该现象 。
23.(12分)在银锌原电池中,以硫酸铜为电解质溶液,锌为 极,电极上发生的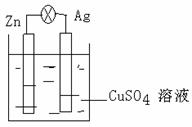 是
反应(“氧化”或“还原”)。电极反应式:
是
反应(“氧化”或“还原”)。电极反应式:
为 ,
锌片上观察到的现象为
银为 极,电极上发生的是 反应(“氧化”或“还原”),
电极反应式是 ,
总的化学方程式
银片上观察到的现象是 。
在整个过程中是 能转化为 。
(2)若反应过程中有0.2mol电子发生转移,则生成的铜为 克。
20.下列说法正确的是( )
A 一个反应是吸热还是放热与反应条件有关
B化学反应中的能量变化都表现为热量的变化
C反应物的总能量低于生成物的总能量时,发生吸热反应
D由H形成1molH-H键要吸收热量
二 填空
21(8分)化学式为C8Hm 的烷烃,m值等于 ;化学式为CnH22的烷烃,n值等于 ,一氯甲烷的化学式 ,其相对分子质量是 。
22按要求填空(8分)
(1)水的电子式 (4)电解氯化铜溶液的化学方程式
(3)氯离子的原子结构示意图 (2)甲烷的结构式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com