
题目列表(包括答案和解析)
7.某原子核外共有n个电子层(n>3),则(n-1)层最多容纳的电子数为
A.8个 B.18个 C.32个 D.2(n-1)2个
6.同种元素的原子和离子,具有相同的
A.质子数 B.电子数 C.电子层数 D.最外层电子数
5.已知某粒子的质子数,则可确定的
A.中子数 B.最外层电子数 C.核电荷数 D.相对原子质量
4.核外电子分层排布的主要原因是
A.电子的质量不同 B.电子的能量不同
C.电子的数量不同 D.电子的大小不同
3.下面关于多电子原子核外电子的运动规律的叙述正确的是( )
A.核外电子是分层运动的
B.所有电子在同一区域里运动
C.能量高的电子在离核近的区域运动
D.能量低的电子在离核远的区域绕核旋转
2. 某元素的原子核外有三个电子层,M层的电子数是L层电子数的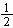 ,则该元素的原子是
,则该元素的原子是
A.Li B.Si C.Al D.K
1.我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的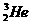 ,每百吨
,每百吨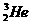 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氮元素主要以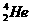 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
A.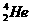 原子核内含有4个质子 B.
原子核内含有4个质子 B.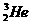 和
和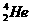 互为同位素
互为同位素
C.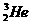 原子核内含有3个中子
原子核内含有3个中子
D.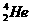 的最外层电子数为2,所以
的最外层电子数为2,所以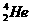 具有较强的金属性
具有较强的金属性
23.(11分) 将标准状况下的11.2L氨气溶于100mL水中,得到密度为0.868 g·cm-3的氨水。(不考虑氨气与水的反应)
(1)该气体的物质的量= mol;溶液的体积= L;
所得氨水的物质的量浓度= mol·L-1。
(2)若取上述氨水30.0mL与70.0mL2.00mol·L-1的AlCl3溶液相混合,产生白色沉淀的质量是 g。
(3)若取某浓度的NaOH溶液50.0mL与50.0mL2.00mol·L-1的AlCl3溶液相混合,有白色沉淀产生,测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的物质的量浓度为 mol·L-1
22.(12分)实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、教育博客碳酸氢铵的氯化钠。某学生设计了如下方案:

如果此方案正确,那么:
(1)操作①可选择_____ 仪器。
A、烧瓶B、烧杯C、锥形瓶D、坩埚 E、蒸发皿
(2)操作②是否可改为加硝酸钡溶液?为什么?
(填能或不能)理由
(3)进行操作②后,如何判断SO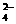 已除尽,方法是__________
已除尽,方法是__________
(4)操作③的目的是_________
为什么不先过滤后加碳酸钠溶液?理由是___________________。
(5)操作④的目的是__________________________________ _。
 19(10分) 已知A、B、C、D、E五种物质有如图
19(10分) 已知A、B、C、D、E五种物质有如图
所示的转化关系(部分反应物及反应条件未列出,
若解题时需要,可作合理假设),且五种物质中均
含有A元素。
(1) 若A为固体非金属单质
①D的化学式为
②C→D的化学方程式
(2)若A为气态非金属单质
① D物质的颜色是
②A→B的化学方程式
③E→C的离子方程式为 。
20(13分)A、B、C、D、E、F都是短周期主族元素,教育博客原子系数依次增大。其中B原子最外层上的电子数是其电子层数的2倍;教育博客A能和C形成原子个数比为1:1和2:1的物质;D也能和C形成原子个数比为1:1和2:1的物质;D、E、F元素的最高价氧化物的水化物两两皆能反应,都生成盐和水;F单质在常温下是一种气体。试回答:
(1)请写出下列元素的名称: C______,E_______, F______, B在元素周期表中的位置是________________。
(2)B、C、F三种元素形成的氢化物中,沸点最高的是________________。(填分子式)
(3)A与C形成的含有18个电子的分子的电子式是_____________。
(4)C、 D单质形成原子个数比为1:1的化合物的化学方程式是_______________。
(5)E单质与D元素最高价氧化物的水化物反应的离子方程式是______________。
21(10分)某溶液中可能含有Na+,K+,Br-,SO42-,CO32-等离子中的全部或其中的几种,现分别取三份溶液,进行如下操作:
a.用洁净的铂丝蘸取溶液在无色火焰上灼烧,火焰呈黄色;
b.溶液中通入氯气,溶液由无色变为橙色;
c.溶液中加入过量的稀硫酸后,无气体放出,再加入Ba(NO3)2溶液后,产生白色沉淀.
(1)原混合液中一定存在的离子是 ,一定不存在的离子是 .
(2)为确定 离子是否存在,只需将c操作中如何改进?______________
(3)为确定 离子是否存在,应补充的实验操作是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com