
题目列表(包括答案和解析)
2.下列说法不正确的是
A.任何反应都伴有能量的变化
B.化学反应中的能量变化都表现为热量变化
C.反应物的总能量高于生成物的总能量时发生放热反应
D.反应热可用△H表示,当△H>0时,表示化学反应为吸热反应
2分,共32分)
1. 2008年8月8日第29届奥运会将在北京举行,下列说法正确的是
A.奥运会场馆“鸟巢”使用的Q460特殊钢属于合金
B.奥运会期间使用的大型遥控飞艇充入的安全且轻的气体是氢气
C.奥运会场馆“水立方”用的新研制涂料氮化镓属于硅酸盐材料
D.奥运吉祥物“福娃”制品内的填充物聚酯纤维是天然高分子材料
28.(16分)已知①一下条件下,R-Cl+2Na+Cl-R′→R-R′+2NaCl
②醛和醇可以发生氧化反应,相关物质被氧化的难易次序是:
 R
R
 RCHO最易,R-CH2OH次之, CHOH最难
RCHO最易,R-CH2OH次之, CHOH最难
R
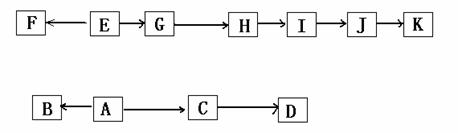 现有某氯代烃A,其相对分子质量为78.5;B与氯气反应生成的一氯代物有两种。
现有某氯代烃A,其相对分子质量为78.5;B与氯气反应生成的一氯代物有两种。
有关的转化关系如下图所示(部分产物及条件均已略去);
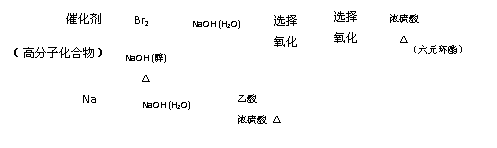
请回答下列问题:
(1)分子式:A ;反应类型:A→C ,E→F ;
(2)结构简式:B ,K ;
(3)反应方程式:A→E 。
G→H 。
(4)D的同分异构体属于羧酸的有四种,其中有2个-CH3基团的有两种。请写出这两种中的任一种结构简式为 。
27.(10分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: ⑴若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是 。在X极附近观察到的现象是 。
 ②Y电极上的电极反应式是 ,检验该电极反应产物的方法是 。
⑵如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
②Y电极上的电极反应式是 ,检验该电极反应产物的方法是 。
⑵如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
26.(12分)某无色透明溶液中可能存在Na+、Ag+、Ba2+、Fe3+、AlO2-、CO32-、SO32-、SO42-,取该溶液进行相关实验,实验结果记录如下:
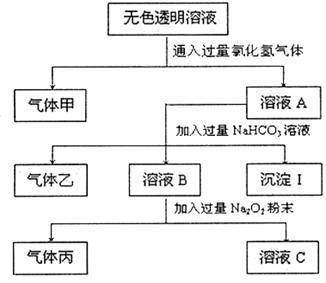
(1)不进行任何化学反应即可判断该溶液中肯定没有的离子是 ;与该离子同元素的单质在气体丙中燃烧的现象是 。将少量含有该离子的氯化物的饱和溶液滴入沸腾的水中生成红褐色液体,反应的化学方程式是
。
(2)为确定气体甲的成分,用下图所示装置实验,若A瓶溶液颜色褪色B瓶溶液中有白色沉淀生成,则甲气体的组成可表示为 。

(3)该无色透明溶液中一定存在的离子是 。
25.(14分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E、F形成的化合物甲、乙、丙、丁、戊、己的组成如下表所示。
|
化合物 |
甲 |
乙 |
丙 |
丁 |
戊 |
己 |
|
化学式 |
A2C |
A2C2 |
B2A2 |
D2C2 |
A2E |
DF |
回答下列问题
(1)化合物丙的电子式为 。化合物丁存在的化学键类型是 。
(2)化合物甲的沸点比戊 (填“高”或“低”),原因是
(3)向含有0.2mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数目为 个。
(4)2.0g丙完全燃烧,生成液态甲和B的气态氧化物,放出99.6KJ的热量,请写出表示丙的燃烧热的热化学方程式
(5)用铁作阳极、石墨作阴极,电解甲、己的混合溶液,电解反应的方程式为:
24.铜既不溶于稀硫酸,也不溶于NaNO3溶液,但可溶于其混合液。现有2mol/L稀硫酸30mL,往其中加入1.7gNaNO3晶体,充分溶解,该混和液最多可溶解铜的物质的量为
A.0.045mol B.0.03mol C.0.0225mol D.0mol
23.食品香精菠萝酯的生产路线(反应条件略去)如下:
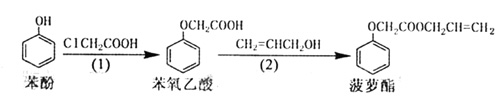
下列叙述错误的是
A.步骤(1)产物中残留的苯酚可用FeCl3,溶液检验
B.苯酚和菠萝酯均可与溴水发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的丙烯醇可用溴水检验
22.下列说法中正确的是
A.在相同条件下,若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨,s)=C(金刚石,s);△H=+1.9kJ·mol-1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ·mol-1,若将含0.5mol H2SO4的浓硫酸与1mol NaOH溶液混合,放出的热量大于57.31 kJ
D.在101Kpa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H=+285.8kJ·mol-1
21.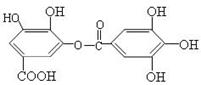 某有机物的结构简式如下图所示,对该有机物的下列叙述中不正确的是
某有机物的结构简式如下图所示,对该有机物的下列叙述中不正确的是
A.常温下,能与Na2CO3溶液反应放出CO2
B.在发生碱性水解时1mol该有机物能消8molNaOH
C.与稀硫酸共热时可生成两种有机物
D. 该有机物的分子式是C14H10O9
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com