
题目列表(包括答案和解析)
18.写出下列反应的热化学方程式。(4分)
(1)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量
____________________________________________________
(2)10g CaCO3分解吸收热量17.56kJ
__________________________________________________
17.(15分)(1)影响化学反应速率的外界条件主要是__________、__________、__________、__________,一般地说,其他条件不变时,__________或__________都可以使化学反应速率增大,而__________对有气体参加或生成的反应有影响。
(2). 在原子序数为1~18的元素中,其单质可以形成原子晶体的元素主要有 ,其单质是金属晶体的有 ,举出三种其单质是分子晶体且在常温下是气体的素 。
16、将下列晶体熔化:氢氧化钠、金刚石、硫化钾、干冰,需要克服的微粒间的相互作用
①共价键 ②离子键 ③分子间作用力,正确的顺序是( )
A.①②②③ B.②①②③ C.②③②① D.①①②③
第Ⅱ卷非选择题部分(共52分)
15、Na和Na+两种粒子中,不相同的是 ①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数( ) A.①② B.②③ C.③④ D.②③④
14.对原电池的电极名称,下列叙述中错误的是( )
A.电子流入的一极为正极 B.比较不活泼的一极为正极
C.电子流出的一极为负极 D.发生氧化反应的一极为正极
13. 4P(红磷s) P4(白磷s);△H=+17kJ·mol-1根据以上方程式,下列推论正确的是( )
4P(红磷s) P4(白磷s);△H=+17kJ·mol-1根据以上方程式,下列推论正确的是( )
A.当lmol白磷转变成红磷时放出17kJ热量
B.当4g红磷转变成白磷时吸收17kJ热量
C.正反应是一个放热反应
D.白磷热稳定性比红磷大
12.在一定条件下,对于在密闭容器中进行的反应P(g)+Q(g)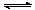 R(g)+S(g),下列说法中可以充分说明这一反应已经达到平衡状态的是( )
R(g)+S(g),下列说法中可以充分说明这一反应已经达到平衡状态的是( )
A.P、Q、R、S的浓度相等 B.P、Q、R、S在容器中共存
C.P、Q、R、S的浓度不再变化 D.P、Q的反应速率相等
10.反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(NH3)=0.010mol/(L·s) B.v(O2)=0.0010mol/(L·s)
C.v(NO)=0.0010mol/(L·s) D.v(H2O)=0.045mol/(L·s)
11 下列物质放入水中,会显著放热的是( )
A.食盐B生石灰C硝酸铵D蔗糖
9. 下列两种物质之间属于同素异形体关系的是
A. 石墨和C60 B. 水和重水
B. 正丁烷和异丁烷 D. 12C 和13C
8. 下列物质中,既有离子键又有共价键的是
A. CaCl2 B. KOH C. H2O D.HF
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com