
题目列表(包括答案和解析)
25.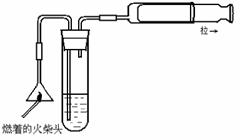 (5分)火柴头中含有硫和氯元素,用适当的方法可加以检验,回答下列问题:
(5分)火柴头中含有硫和氯元素,用适当的方法可加以检验,回答下列问题:
(1)右图是检验火柴头中含有硫元素的实验装置示意图。图中试管中应装有 溶液,拉动注射器活塞时,若观察到 现象
证明火柴头燃烧时产生了 。
(2)原火柴头中的氯元素是以KClO3的形式存在的,其作用是助燃剂, 当火柴头燃烧后其中的氯元素是以 物质的形式存在,检验的方法 。
24.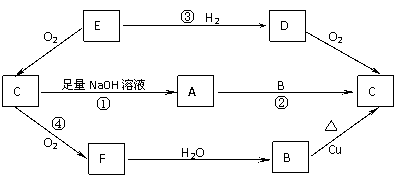 (9分)下图是六种物质的相互转化关系,已知E是固体单质,六种物质均含有E元素。
(9分)下图是六种物质的相互转化关系,已知E是固体单质,六种物质均含有E元素。
(1)写出各物质的化学式: B ;E ;F ;
(2)写出反应①的离子方程式________________________________________
(3)写出反应④的化学方程式_________________________________________
(4)写出B→C反应的化学方程式
23.(6分)今有两个氢气燃烧生成水的热化学方程式
H2(g) + 1/2O2(g) == H2O(g) △H=a kJ/mol
2H2(g) + O2(g) == 2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:︱b︱表示b的绝对值)
(1)若2 mol H2完全燃烧生成水蒸气,则放出的热量 ︱b︱kJ(填“>”、“<”或“=”)
(2)反应热的关系:2a b(填“>”、“<”或“=”)。
(3)若已知H2(g) + 1/2O2(g) == H2O(g) △H=-242 kJ/mol ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol
H-H键断裂时吸收的热量为
22.(10分)A、B、C、D、E、F都是短周期元素,原子序数依次增大。
|
元素 |
有关信息 |
|
A |
原子最外层电子数和电子层数相等 |
|
B |
原子的最外层电子数是内层电子数的2倍 |
|
C |
元素主要化合价为-2,原子半径为66pm |
|
D |
与A同主族,最高价氧化物对应的水化物易溶于水 |
|
E |
原子半径为104pm,所在主族序数与所在周期序数之差为3 |
|
F |
单质为有色的气体 |
(1)D2C的电子式 ;
(2)沸点:A2C A2E(填“>”或“<”或“=”);
(3)E的非金属性比F (填“强”或“弱”),并用化学事实加以说明(用化学方程式表示) ;
(4)化合物甲由A、B、C、D四种元素组成,其化学式量为84,是焙制糕点所用发酵粉的主要成分之一。写出甲在水溶液中与盐酸反应的离子方程式 。
21.(4分)有以下各组微粒或物质:
A.正丁烷和异丁烷; B.金刚石、石墨和C60
C.O2和O3; D.35Cl和37Cl; E.乙醇和二甲醚;
其中,互为同分异构体的有 (填编号,以下同);互为同素异形体的有 。
20.已知可逆反应:N2(g) + 3H2(g)
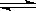 2NH3(g) △H=-92 kJ·mol-1下列关于此反应的说法中错误的是
2NH3(g) △H=-92 kJ·mol-1下列关于此反应的说法中错误的是
A.加压可使该反应的反应速率变大
B.该反应中反应物的总能量比生成物的总能量高
C.将1 mol N2和3 mol H2混合进行反应,反应完成时放出的热量为92 kJ
D.单位时间内生成1mo lN2,同时消耗3 mol H2说明该反应达到平衡状态
19.现有如下各说法:

①在水分子中氢、氧原子间以共价键相结合
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl = H+ + Cl-,判断HCl分子里存在离子键;
⑤冰的密度比水的密度小,这与氢键有关
上述各种说法正确的是
A.①②⑤ B.①②④⑤ C.①②③④⑤ D.①③④⑤
18.下列物质中,既含有离子键,又含有非极性键的是
A.NaOH B.Na2O2 C.MgCl2 D.H2O2
17.氢气是很有前途的能源物质,以水为原料大量制取氢气的最理想的途径是
A.以焦炭和水制取水煤气分离出氢气 B.利用太阳能直接使水分解产生氢气
C.用铁和盐酸反应放出氢气 D.由热电站提供电力电解水产生氢气
16.将相同表面积的纯锌片和纯铜片按图所示同时插入相同浓度的稀硫酸中,以下有关叙述正确的是
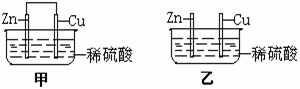
A.甲装置中电能转化为化学能 B.乙装置产生气泡速率比甲装置快
C.乙装置中铜片上发生 2H++2e-= H2↑ D.甲装置中铜片表面有气泡产生
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com