
题目列表(包括答案和解析)
1.我国政府规定,自6月1日起,所有超市、商场、集贸市场等一律不得免费提供塑料购物袋。据了解,一次性塑料袋大多是聚氯乙烯和聚苯乙烯制成的再生塑料制品,对人体是有害的。下面对一次性塑料袋的说法错误的是
A.一次性塑料袋是链状结构的高分子材料 B.禁止使用任何塑料制品
C.一次性塑料袋是有机物组成的 D.一次性塑料袋是“白色污染”之一
33.(6分)某化学活动小组用稀盐酸对赤铁矿Fe2O3含量进行测定(杂质不与盐酸反应且不溶于水),得到一黄色残液。为防止直接排放造成环境污染,对其组成进一步进行探究。过滤该残液,取100 g 滤液,向基中不断加入5%和氢氧化钠溶液,所得实验数据如下表:
|
加入氢氧化钠的溶液的质量/g |
20 |
40 |
60 |
80 |
160 |
180 |
|
生成沉淀的质量/g |
0 |
0 |
0.80 |
1.78 |
5.35 |
5.35 |
(1) 通过对上述实验数据的分析,该滤液中含有的溶质是--------------(写化学式)。
(2) 选择合理的数据,计算100 g 滤液中溶质的质量(若有多种溶质,任选一种。结果精确到0.01g)。
可能用到的相对原子质量:H-1 O-16 Na -23 Cl-35.5 Fe -56
32.(6分)现有甲、乙两包白色固体,已知甲中含有NaCl、NaNO3、NaCO3、NaOH中的一种或几种,乙为纯净物,是初中化学学习中涉及到的物质。为了证明甲、乙两包固体的成分,现进行如下实验:
(1)实验一
|
操作步骤 |
实验现象 |
结论 |
|
①取甲中少量粉末加足量水充分溶解 |
溶液呈无色 |
---------- |
|
②取①中所得溶液少量,滴加紫色石蕊试液 |
石蕊试液变了蓝色 |
溶液pH----7(填“>”、“<”或“=” |
|
③另取①中所得溶液少量,滴加稀盐酸 |
无明显现象 |
甲中一定含有------(填化学式,下同),一定不含有------,可能含有--------。 |
(2)实验二(部分物质在流程图中未列出)
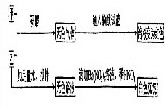
根据以上实验推断,乙物质为-----------(填写化学式),使用该物质时应注意---------------。
31.人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产的需要。
(1)钢铁是我们日常生活中使用最多的金属材料。高炉炼铁常以焦炭、铁矿石、石灰石、空气等为原料。炼铁过程中,一氧化碳和赤铁矿(主要成分为Fe2O3)反应的化学方程式为-----------------------------。
(2)我国钢铁年产量很高,但因锈蚀造成的损失也很惊人。人们常采取在铁制品表面涂刷油漆或镀上其他金属等方法,以防止其锈蚀。上述方法所依据的原理是----------------- 。
(3)我国矿物储量很丰富,但人均占有量并不多,请保护金属资源!下面几种做法中,可有效保护金属资源的是-------------------(填字母)。
a.回收利用废旧金属制品
b.任意开采铁矿石
c.铁制品不加处理,存放在潮湿的环境中
d.寻找、开发金属的代用品
30.(5分)根据下列的实验装置图回答问题。
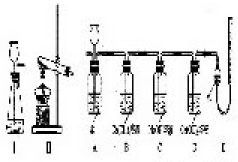
(1) 装置Ⅰ在实验中可用于过氧化氢溶液制氧气,其反应的化学方程式为------------------。
(2) 在化学实验中,对装置稍加改装或采用不同的组合时,就能完成多种实验。如将装置Ⅱ改为Ⅳ后,可以顺利进行草酸受热扫解的实验。
草酸是一种有机物,常温时为一种无色透明的晶体,加热时易分解。草酸受热分解的化学方程式为:C2H2O2==H2O+CO2+CO
根据改进后图Ⅳ所示实验装置推测草酸还具有的物理性质为-------------------。
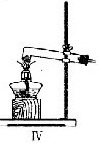
(3) 现将装置Ⅳ与装置Ⅲ相连,对草酸受热分解后所得产物的组成和性质进行探究。实验开始前E中左右液面在同一水平面上。
① 装置Ⅲ中A可用于收集反应生成的水,还具有------------的作用;
② 实验过程中,D中一直无明显现象,E中球容器内液面-----------(填“升高”、“降低”或“不变”)。
29.(4分)燃料燃烧所产生的热量给生活与生产带来了很大的便利,但燃烧不当也会造成极大的损害。
(1)燃烧不完全燃烧既浪费资源,产生的气体又对环境造成污染。为研究影响物质燃烧的因素,现设计如下图所示实验:
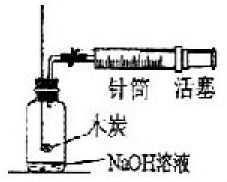
将燃烧匙内小木炭块灼烧至红热后,立即伸入集气瓶内,并塞紧橡皮塞。将注射器内氧气迅速推入集气瓶内,观察到木炭发白光。该实验说明燃烧的剧烈程度与---------有关。
燃烧的剧烈程度还与可燃物与氧气的接触面积有关,如----------(举一日常生活实例)
(2)小明、小刚同学在研究灭火的原理时,进行了如下实验:分别在两个小铁盒中倒入少量植物油并点燃,小明用坩埚钳把小铁盒放在冰水共存的水面上,观察到火焰立即熄灭,该实验证明了灭火的原理是-----------,小刚同学将一块湿抹布盖在小铁盒上,火焰也立即熄灭,他依据的灭火原理是----------。
28.(3分)下表是元素周期表中的部分信息,A、B、C、D分别是4种粒子的结构示意图。请根据图中信息及相关要求真空。
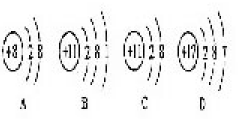

(1) 硫元素的原子的核外电子数为---------------。
(2) A、B、C、D 4种粒子中,易得到电子,形成稳定结构的是--------------(填字母序号)。
(3) 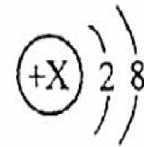 某离子带2个单位正电荷,
某离子带2个单位正电荷,
其结构示意图如下图,该离子的符号是-----------。
27.(3分)有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如Ca(OH)2,Ba(OH)2的溶解度就存在一定的差异,如下表所示:
|
温度/℃ |
0 |
40 |
80 |
|
|
溶解度/g |
Ca(OH)2 |
0.187 |
0.141 |
0.094 |
|
Ba(OH)2 |
1.67 |
8.22 |
101.4 |
根据以上信息回答下列问题。
(1) 下图中,表示Ca(OH)2溶解度曲线的是-----------( 填“A”或“B”)。
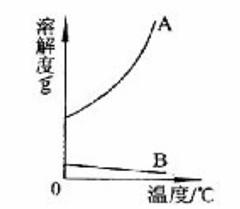
(2) 如果要将Ca(OH)2的不饱和溶液转为饱和溶液,可采取的方法是--------------(只举一种)
(3) 现有常温时含Ca(OH)2,Ba(OH)2两种溶质的某饱和溶液,若要得到较纯净的Ba(OH)2溶液,采取的物理方法为-----------------。
26.(4分)按要求用相应的化学符号填空。
(1)洒精---------
(2)两个氢离子-------------
(3)地壳中含量最多的元素--------------------
(4)写出五氧化二磷的化学式,并标出其中磷元素的化合价---------------
7.下图中,施工人员正在为紧邻居民区的轻轨轨道安装封闭的隔音屏,尽量将列车产生的噪声降低到最低限度。这种控制噪声的方式是( )。
 A.防止噪声产生
A.防止噪声产生
B.阻断噪声的传播
C.防止噪声进入耳朵
D.采用了上述三种方式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com