
题目列表(包括答案和解析)
5.某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,则该金属可能为
( )
A.铝 B.铜 C.锡 D.硅
4.据报导我国最近合成多种元素的新同位素,其中一种是
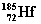 (铪),它的中子数是( )
(铪),它的中子数是( )
A.72 B.113 C.185 D.257
3. 反应A(g)+3B(g) 2C(g)+ 2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是
反应A(g)+3B(g) 2C(g)+ 2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是
A.v(C)= 0.04 mol /(L·S) B.v(B)= 0.06 mol /(L·min)
C.v(A)= 0.15 mol /(L·min) D.v(D)= 0.01 mol /(L·S)
2.下列过程中,把化学能转化为热能的是 ( )
A.风力发电 B.干电池产生电流
C.木炭燃烧 D.用电取暖器取暖
1.可燃冰是天然气与水相互作用形成的晶体物质,主要存在于冻土层和海底大陆架中。据测定每0.1m3固体“可燃冰”能释放出20m3甲烷气体,则下列说法中不正确的是( )
A.“可燃冰”释放的甲烷属于烃
B.“可燃冰”是水变油,属于化学变化
C.“可燃冰”将成为人类的后续能源
D.储量巨大的“可燃冰”的分解与释放,会诱发海底地质灾害,还会加重温室效应。
15.8.70g MnO2与100mL 37.0%密度为1.19g/cm3的浓盐酸共热(假设HCI没有损失),反应结束后,将剩余的溶液加水稀释至100mL。取出10mL溶液加入足量AgNO3溶液,有白色沉淀生成。求(1)反应中生成的Cl2在标准状况下的体积.
(2)10.0mL溶液加入AgNO3溶液后生成沉淀的质量.
13.(12分)在100℃时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如下表格:
|
时间(s) 浓度 (mol·L-1) |
0 |
20 |
40 |
60 |
80 |
100 |
|
C(N2O4) |
0.100 |
C1 |
0.050 |
C3 |
a |
b |
|
C(NO2) |
0.000 |
0.060 |
C2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为 ,达到平衡时,四氧化二氮的转化率为 ,表中C2 C3,a b(填“>” 、“<” 或“=” )
(2)20s时四氧化二氮的浓度C1= mol·L-1,在0-20s时间段内,四氧化二氮的平均反应速率为
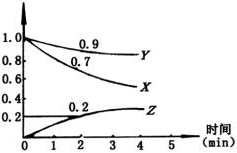
14.(10分) 某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。
(1)由图中数据分析:该反应的化学方程式为 。
(2)反应开始至2min,用Z表示的平均反应速率为 。用X表示的平均反应速率为 。
(3)判断:第5分钟时,反应是否达到平衡?_______.第5分钟时,Z的生成速率与Z的消耗速率相比_________(填”大”、“小”或“相等”)
11.(12分))回答有关氯气制备的几个问题
实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2O。现有两个同学分别设计的两套实验装置如下图:
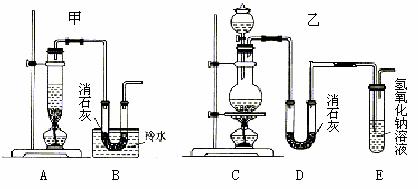
(1)写出制取氯气的化学方程式 。
(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的
选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。
|
|
优 点 |
缺 点 |
|
甲装置 |
|
|
|
乙装置 |
|
|
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分连接顺序是 (按气流流动的方向) 。该组合中还缺少的装置是 ,原因是 。
(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过 mol。
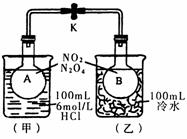 12(6分).如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲中盛放100 mL 6 mol/L的HCl溶液,烧杯乙中盛放100 mL冷水。现向烧杯甲的溶液中放入25 g NaOH固体,同时向烧杯乙中放入25 g NH4NO3固体,搅拌使之溶解。
12(6分).如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲中盛放100 mL 6 mol/L的HCl溶液,烧杯乙中盛放100 mL冷水。现向烧杯甲的溶液中放入25 g NaOH固体,同时向烧杯乙中放入25 g NH4NO3固体,搅拌使之溶解。
⑴A瓶中气体颜色 ,理由是 。
⑵B瓶中气体颜色 ,理由是 。
10.下列关于原电池的叙述中正确的是( )
A.正极和负极必须是两种不同的金属
B.原电池是把化学能转化成电能的装置
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5g锌溶解,正极上就有0.1g氢气生成
9.A、B、C都是金属,把A浸入C的硝酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
A.A>B>C B.A>C>B
C.B>A>C D.B>C>A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com