
题目列表(包括答案和解析)
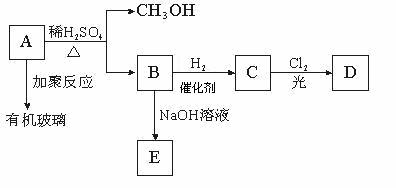
28.(18分)有机玻璃是一种重要的塑料,它是由有机物A发生加聚反应得到的,有机物A(C4H6O2)能使溴水褪色且可以发生水解反应:
请回答:
(1)B分子中含有的官能团名称是
(2)由B转化为C的反应属于 反应
(3)D为C的一氯代物,且有两种结构,写出D的结构简式 ;
(4)由B生成E的化学方程式是
(5)有机玻璃的结构简式是
26. (15分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式______________________________。
 (2)若将(1)中的反应设计成原电池,原电池的装置图如右,请写出电极反应式。
(2)若将(1)中的反应设计成原电池,原电池的装置图如右,请写出电极反应式。
负极反应__________________________________;
正极反应__________________________________。
(3)FeCl3中常混有FeCl2,请写出除去FeCl2的离子方程式________________________;
(4)请任写出一种检验Fe3+的试剂__________________________。
|
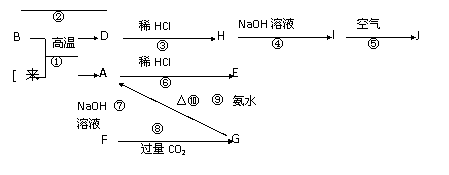
则⑴写出物质的化学式B F G
⑵写出反应①、④、⑦的化学方程式:
① ;
④ ;
⑦
25. 碱性电池有容量大、放电电流大的特点。锌-锰碱性电池以氢氧化钾溶液为电解液,总反应式为: Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池负极的电极反应式为:Zn(s) -2e-+2 OH- = Zn(OH)2(s)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g
Ⅱ卷(60分)
24.将质量分数是3a%和a%的两种溶液等体积混合后,混合液的质量分数小于2a%,则该溶液的溶质可能是( )
A.H2SO4 B.NaCl C.C2H5OH D.NH3·H2O
23.能说明某烃分子里含有碳碳不饱和键的叙述中正确的是 ( )
A.分子组成中含碳氢原子数比为1:2
B.完成燃烧生产等物质的量的CO2和H2O
C.能与溴加成反应而使溴水褪色,还能使KMnO4酸性溶液褪色
D.空气中燃烧能产生黑烟
22.在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应:
A(s)+3B(g)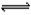 2C(g)+D(g)已达平衡的是 ( )
2C(g)+D(g)已达平衡的是 ( )
A.混合气体的压强 B.混合气体的密度 C.A的物质的量浓度 D.气体总物质的量
21、反应2SO2+O2
 2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
A.0.1s B.2.5s C.5s D.10s
20. 有一无色溶液,可能含有K+、Al3+、Mg2+、Cl-、SO42-、MnO4-中的一种或几种。为确定其成分,做如下实验:①取部分溶液,加入适量NaOH溶液后生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
A、肯定有K+、MnO4- B、肯定有Al3+、Mg2+、Cl-
C、肯定有Al3+、Mg2+、SO42- D、肯定有K+、Al3+、Mg2+、SO42-
19.取5g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了5g。下列物质中不能满足上述结果的是( )
A、H2 B、CO C、C6H12O6 D、C12H22O11
18.氯化碘(ICl)的性质类似卤素,有很强的化学活动性。ICl跟Zn、H2O的反应如下:
①2ICl+2Zn=ZnCl2+ZnI2 ②ICl+H2O=HCl+HIO 下列叙述中正确的是( )
A.在反应①中,ZnI2既是氧化产物又是还原产物
B.在反应①中,ZnCl2既是氧化产物又是还原产物
C.在反应②中,ICl既是氧化剂又是还原剂
D.在反应②中,ICl既不是氧化剂,又不是还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com