
题目列表(包括答案和解析)
31、某溶液中含有SO42-、CO32-、OH-三种阴离子,如果只取一次溶液,分别将三种离子检验出来。
(1)先检验____ __,加入__ ___试剂;

 w_w w. k#s5_
w_w w. k#s5_
(2)再检验___ ___,加入___ __试剂。
(3)最后检验______,加入_______试剂。
23.(10分) A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 。D的最高价氧化物的水化物是 。
(2)写出A、B的化合物与E反应的化学方程式:
(3)A、B两元素形成化合物属 (“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:
22.(14分)下表是元素周期表的一部分,请回答有关问题:
|
主族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
① |
② |
|
③ |
|
|
3 |
|
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
④ |
|
|
|
|
⑩ |
|
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式
(3)④元素与⑦元素形成化合物的电子式
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是
(填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
|
实验步骤 |
实验现象与结论 |
|
|
|
19(6分)、下列五种物质中,①Ar ② ③
③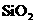 ④NaOH ⑤
④NaOH ⑤ ,只存在共价键的是
,只存在离子键的是
,既存在离子键又存在共价键的是
,不存在化学键的是 。属于共价化合物的是
属于离子化合物的是
。(填序号)
,只存在共价键的是
,只存在离子键的是
,既存在离子键又存在共价键的是
,不存在化学键的是 。属于共价化合物的是
属于离子化合物的是
。(填序号)
20(7分). 已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液: 溶液、
溶液、 溶液、盐酸。按要求回答下列问题:
溶液、盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
,若能,请写出电极反应式,负极 ,正极 。(若不能,后两空不填)
(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池的正负。)
21.(9分)某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。
|
实验方案(I)[ |
实验现象(Ⅱ) |
答案(III) |
|
|
实验方案I |
实验现象II |
||
|
1.用砂纸擦后的镁带与沸 水反应,再向反应液中滴 加酚酞 |
A浮与水面,剧烈反应,放出气体, 熔成-个小球,在水面上无定向移 动,随之消失,溶液变红色。 |
1 |
|
|
2.向新制的H2S饱和溶 液中滴加新制的氯水 |
B.产生大量气体,可在空气中燃 烧,溶液变成浅红色 |
2 |
|
|
3.钠与滴有酚酞的冷水反应 |
C.反应不十分剧烈,产生的气体 可以在空气中燃烧 |
3 |
|
|
4.镁带与2mol/L的盐酸 反应 |
D.剧烈反应,产生的气体可以在 空气中燃烧 |
4 |
|
|
5铝条与2mol/L的盐酸 反应 |
E.生成白色絮状沉淀,继而沉淀 消失 |
5 |
|
6.向AlCl3溶液中滴加 溶液至过量 溶液至过量 |
F.生成淡黄色沉淀 |
6 |
|
(2)通过以上实验分析了同周期元素的符号 ,从实验结果可以得出的结论是 。
40.(10分)A、B是两种常见的无机物,它们分别能与下图中周围4种物质在一定条件下反应:

请回答下列问题:
(1)A溶液与B溶液反应的离子方程式 。
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为____________________________________________________
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:
,
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:
__________________________________
39.(10分)下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
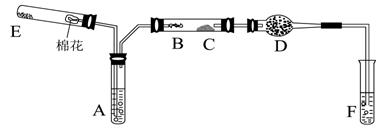
图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
D处使用碱石灰的作用是 。
(3)检验乙醇氧化产物时F中的实验现象是 。
(4) E处是一种纯净物,其反应方程式为 。
(5)写出乙醇发生催化氧化的化学方程式 。
38.(9分)X、Y、Z三种短周期元素,两两之间能组成5种化合物A、B、C、D、E;X、Y、Z三种元素可组成化合物F。已知:化合物A、B、C中原子个数比都为1︰1;B为淡黄色固体,C、E常温下均为无色液体;A是化学式为XZ的离子化合物,A与E反应生成F和一种气体;D是化学式为X2Y的离子化合物,D的阴、阳离子具有相同的电子层结构且与E分子所含电子 数相等。 请回答下列问题:
(1)X元素的名称是________________
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)____________________
(3)写出F的电子式______________________________
(4)已知X单质、A、B、D固体,分别与E反应都生成同一种物质,其中X单质、A、B分
别与E的反应均是氧化还原反应。请写出X单质、B分别与E反应的化学方程式
__________________________________, ;
B中含有的化学键是 ;
请举一例说明B的用途______________________________________________________
(5)请写出由化合物C制取Y的单质反应的化学方程式_______________________________
37.(6分)已知某烃A含碳元素的质量分数为85.7%。结合以下信息回答问题:
(1)若烃A密度是相同状况下氢气密度的42倍。
则烃A的相对分子质量_____________,分子式为_____________。
(2) 若烃A可作果实催熟剂。
则由A制取高分子化合物的化学方程式为
A和水在一定条件下反应生成B。B为生活中常见的有机物,B可与另一种生活中常见有机物在一定条件下反应生成有香味的物质C,写出生成C的化学方程式
36.(5分)下列各组物质:
① O2和O3 ; ② 1H、2H、3H; ③ CH4和C10H22; ④乙烷和(CH3)2CHCH2CH3;
⑤  和
和 ;⑥
;⑥ 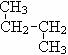 和
和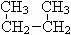
⑦
CH3 (CH2) 3 CH3和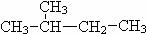
(1)互为同位素的是 ;(2)互为同素异形体的是 ;(3)互为同系物的是 ;
(4)互为同分异构体的是 ;(5)属于同一物质的是 。
35.现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是( )
A.  B.
B. C.
C. D.
D.
Ⅱ卷(共40分,请将正确答案填写在答卷纸的相应位置上。)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com