
题目列表(包括答案和解析)
24.关于反应3NO2+H2O=2HNO3+NO ,下列说法错误的是 ( )
A.氧化剂和还原剂的质量比为2:1
B.氧化产物是HNO3,还原产物是NO
C.每3mol NO2参加反应,必有2mol电子发生转移
D.氧化剂和还原剂都是NO2
23. 在电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是 ( )
A. 将盐酸逐滴加入食盐溶液
B. 将硫酸逐滴加入氢氧化钡溶液
C. 将硫酸逐滴加入氢氧化钠溶液
D. 将醋酸逐滴加入氨水(NH3·H2O为弱电解质,CH3COONH4为强电解质)
22.下列各反应,能用同一离子方程式表示的是 ( )
A. 醋酸和氢氧化钠溶液 醋酸和氨水
B. 氯化钡溶液与硫酸铜溶液 氢氧化钡溶液与硫酸铜溶液
C. 氢氧化钡与稀硫酸 氢氧化钡与稀盐酸
D. 石灰石与稀硝酸 石灰石与稀盐酸
21.实验室中所用少量氯气是用下列方法制取的:
4HCl(浓)+MnO2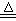 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
(1)该反应既是离子反应也是氧化还原反应。该反应的还原剂是 (用化学式表示)。
写出该反应的离子方程式 。
(2)若有8.7gMnO2与足量的浓盐酸(密度为1.19g·cm-3、HCl的质量分数为36.5%)充分反应后, 共转移电子________摩尔;可制得标准状况下的Cl2________升;被氧化的HCl_______克。(相对原子质量: H-1 O-16 Cl-35.5 Mn-55)
B卷(满分50分)
20.
(8分) 2007年2月27日某市工商局查获400克袋装中老年补钙营养奶粉1401包。这种奶粉被鉴定为所含亚硝酸盐残留量高出正常值7.8倍,长期食用可能致癌。NaNO2有像食盐一样的咸味。已知NaNO2能发生如下反应:2NaNO2 +
4HI 2NO
+ I2 + 2NaI+ 2H2O
2NO
+ I2 + 2NaI+ 2H2O
(1)上述反应中氧化剂是
,若有0.75mol的还原剂被氧化,则被还原的氧化剂是
mol
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①自来水 ②碘化钾淀粉试纸 ③淀粉 ④白糖 ⑤食醋 ⑥白酒。
进行实验时,必须选用的物质有
 (填序号)
(填序号)
(3)某厂废切削液中,含2%-5%的NaNO2,直接排放会造成污染,下列试剂中能使NaNO2转化为不引起二次污染的N2有 (填序号)。
① NaCl ② NH4Cl ③浓H2SO4 ④Cl2
19.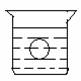 (6分)如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。试回答: K^S*5U.C#
(6分)如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。试回答: K^S*5U.C#
⑴此实验中,观察到的现象有:
① ,
② 。
⑵写出实验过程中反应的离子方程式为
。
18.(9分)(1)下列4组物质均有一种物质的类别与其它三种不同
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3
①以上四组物质中类别不同的物质依次是(填化学式)
A ______;B __;C ;D 。
②这四种物质相互作用可生成一种新物质(碱式碳酸铜,化学式Cu2(OH)2CO3)该反应__________氧化还原反应(填“是”或“否”)。
(2)对于司机酒后驾车,可取其呼出的气体进行检验而查出,所利用的化学方程式如下:
2 CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O,该反应被检测的气体是 ;上述反应中的氧化剂是 (用化学式表示)
17. (16分) (1)写出下列物质在水溶液中的电离方程式:
①硫酸 _______________________________ ②氢氧化钡____________________________
③硫酸铁______________________________
(2)写出下列物质分别与稀盐酸反应的离子方程式:
①实验室用锌和稀硫酸制取氢气:_____________________________________________
②氢氧化铝治疗胃酸过多:___________________________________________________
③用氢氧化钠溶液吸收有毒的氯气 _____________________________________
(3)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组: 。B组: 。
16.向氯化铁溶液中加入过量的铜粉,反应结束后,溶液中大量存在的金属离子是( )
A.Cu2+ Fe2+ B.Fe2+ Fe3+ C.Fe3+ Cu2+ D.只有Fe2+
15.对溶液中的离子反应,下列说法:①不可能是氧化还原反应;②只能是复分解反应;③可能是置换反应;④不能有分子参加。其中正确的是 ( )
A.①③ B.③ C.①② D.③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com