
题目列表(包括答案和解析)
6.电子总数相等的粒子叫做等电子体,下列各组粒子中不属于等电子体的是
A. CH4 与NH3 B.CO2 与HCl C.Ca2+与Cl- D.OH-与NH2-
5.已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是
A.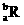 B.
B.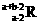 C.
C.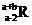 D.
D.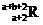
4.下列关于ⅦA族元素的叙述正确的是
A.ⅦA族元素是同周期中原子半径最大的元素
B.ⅦA族元素是同周期中非金属性最弱的元素
C.ⅦA族元素的最高正价都是+7价
D.ⅦA族元素其简单阴离子(X-)的核外电子层数等于该元素所在的周期数
3.下列关于铯(Cs)及其化合物的性质的说法中正确的是
A.金属铯的熔点比金属钠高 B.CsOH比NaOH的碱性弱
C.Cs与H2O能剧烈反应,甚至发生爆炸 D.碳酸铯难溶于水
2.元素性质呈周期性变化的根本原因是
A.元素原子半径大小呈周期性变化
B.元素相对原子质量依次递增
C.元素原子最外层电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
1.在元素周期表中,第一、二、三周期中所含元素种数分别为
A.2、8、8 B.8、8、18 C.2、8、18 D. 8、18、18
25.(9分)7.2g的某烃,完全燃烧产生11.2L(标况下)CO2和10.8gH2O。
(1)该烃中碳、氢两元素的原子个数之比是________。
(2)该烃的分子式是___________________。
(3)该烃可能的结构有________种;若该烃的一氯代物只有一种,则该烃的结构简式是_________________。
忻州市2009-2010学年第二学期高中联考
24.(12分)绿色化学的最大特点在于从开始生产时就采取了污染防治的科学手段,实现生产过程的零污染和生产终端的零污染排放,要实现这种生产方式,就必须充分利用资源中的每一个原子,这种理想的生产方式又被称为“原子经济性”。 现有甲、乙、丙3个化肥厂生产尿素,所用的原料不同,但生产的流程相似,其中第①反应都是在一定条件下含碳原料与水的反应:
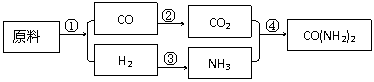
甲厂:以焦炭、空气和水为原料
乙厂:以天然气、空气和水为原料
丙厂:以石脑油(主要成分C5H12)、空气和水为原料
试回答下列问题:
(1)用化学方程式表示乙厂合成尿素的生产过程。
①_______________________________________
②_______________________________________
③_______________________________________
④_______________________________________
(2)3个化肥厂的原料利用率各不相同,试判断化肥厂对原料的利用率最高的是________,简述原因_______________________________________
23.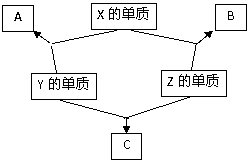 (12分)X、Y、Z三种短周期元素,它们的原子序数之和为16。三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如右图所示变化。已知一个B分子中含有的Z元素的原子个数比C分子中少一个。
(12分)X、Y、Z三种短周期元素,它们的原子序数之和为16。三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如右图所示变化。已知一个B分子中含有的Z元素的原子个数比C分子中少一个。
请回答下列问题:
(1)X元素在周期表中的位置是 ;Y单质的电子式为 。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由空隙中逸出,并在电极表面放电,则正极通入 (填物质名称);负极电极反应式为 。
(3)A与C在一定条件下反应,该反应是消除硝酸工业尾气污染的原理,其化学方程式是
(4)X、Y、Z三种元素可组成一种强酸W与C反应的离子方程式为:
22.(10分)有X、Y、Z三种元素,已知:①X、Y为短周期元素,且X2-、Y-两种离子均具有相同的电子数;②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液显红色。试回答:
(1)X的最高价氧化物对应水化物的化学式是
(2)将ZY3溶液滴入沸水可得到红褐色胶体,反应的离子方程式是 ,光束通过该液体时形成光亮的“通路”,该现象叫____________。
(3)Na2X的电子式为
(4)X的低价氧化物与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制备氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023 个电子转移时,该反应的化学方程式是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com