
题目列表(包括答案和解析)
26.(共11分)现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥E、C同主族,且E比C多两个电子层,E单质可与冷水反应生成氢气。
试回答:
⑴写出元素D、E的名称:D、__________;E、__________。
⑵画出A的原子结构示意图___________________,B的离子结构示意图______________________,D元素位于元素周期表第 周期第 族。
⑶写出B2A3分别与盐酸和氢氧化钠溶液反应的离子方程式:
;
⑷比较B、C、E三种元素形成的简单离子半径的大小和氧化性的强弱(用离子符号表示):
离子半径:____________________;氧化性:_____________________。
⑸写出E与冷水反应的化学方程式: _。
25.(4分)A、B两种气体都是大气污染物,严禁排放,工业上常用碱液吸收。已知A具有还原性,B是一种单质,其水溶液都具有漂白作用。
(1)A是 B是 ,组成B物质的元素的原子结构示意图
(2)若A、B同时作用于一潮湿的有色布条上,其漂白效果会 (选填增强、减弱、不变)
24.(5分) 在O、S、Se、Te四种元素中,单质氧化性最强的化学式是______,简单阴离子还原性最强的离子符号为______. 硒元素最高价氧化物的水化物的化学式为______,它与足量的氢氧化钠溶液反应的化学方程式为______________________________.
23. (8分)下表是元素周期表的一部分, 针对表中的①-⑨种元素,填写下列空白:
|
主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
|
2 |
|
|
|
① |
② |
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
|
|
(1) 在这些元素中,化学性质最不活泼的是: (填具体元素符号,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的电子式是:_____________;
(3) 用电子式表示元素⑦的单质分子的形成过程: ;
(4) 用电子式表示元素④与⑥的化合物的形成过程: ,该化合物属于 (填 “共价”或“离子”)化合物。
(5)表示①与⑦的化合物的电子式 ,该化合物是由 (填“极性”“非极性”下同)键形成的。
22. 用化学符号表示符合下列条件的微粒:(3分)
(1)含有10个电子的分子有: Ne、 HF 、_______、 和 CH4 。
(2)含有10个电子的阳离子有: Na+、______、______、 NH4+和 H3O+。
(3)含有10个电子的常见阴离子有:______、______、和 OH-。
21.写出下列物质的电子式:(4分)
K2S H2O2 NaOH NH4Cl
20.同周期的X、Y、Z三种元素,已知其高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是
A.原子半径:X>Y>Z B.单质的非金属性:X>Y>Z
C.气态氢化物稳定性:X<Y<Z D.原子序数:X<Y<Z
19.已知X、Y均为1-18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则两种元素的原子序数之和为( )
A.19 B.18 C.17 D.9
18.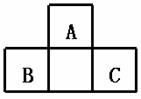 A、B、C均为短周期元素,它们在周期表中的位置如右图.已知B、C两元素在周期表中族
序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 所在的一组是
A、B、C均为短周期元素,它们在周期表中的位置如右图.已知B、C两元素在周期表中族
序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 所在的一组是
A.Be、Na、Al B.B、Mg、Si C.O、P、Cl D.C、Al、P
17.某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为
A.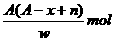 B.
B.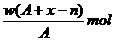
 C.
C.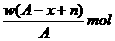 D.
D.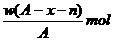
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com