
题目列表(包括答案和解析)
11.(12分)A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;E具有强氧化性。请回答:
(1)用化学符号表示上述5种微粒:
A_________,B_________,C_________,D_________,E_________。
(2)在水溶液中A跟B反应的离子方程式是:_____。
10.(8分)短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)X元素的名称是________;Y元素的名称是________;Z元素的名称是:________。
(2)XZ3化合物的分子式是_________,电子式是_________。
(3)分别写出X、Y的含氧酸的分子式_________、_________。
9.下列事实是由于氯的非金属性比硫强的结果的是
A.次氯酸的酸性比硫酸弱 B.氯能置换硫化氢中的硫
C.常温下单质硫为淡黄色固体,而氯气为黄绿色气体
D.硫能在空气中燃烧,而氯则不能
8.右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
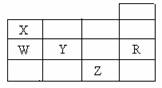 A.常压下五种元素的单质中,Z单质的沸点最高
A.常压下五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
7.居里夫人发现的镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质描述不正确的是
A.在化合物中呈+2价 B.单质能使水分解,放出氢气
C.氢氧化物呈两性 D.碳酸盐难溶于水
6.用元素周期律分析下面的推断,其中错误的是
A.铍(Be)的氧化物对应的水化物可能具有两性
B.砹(At)为有色固体,HAt不稳定
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是比硫化氢稳定的气体
5.砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是
A.AsH3比NH3稳定 B.可以存在-3、+3、+5等多种化合价
C.As2O5对应水化物的酸性比H3PO4弱 D.磷的氧化性比砷强
4.在高温超导体中,铊(T1)是其中成分之一,已知铊是铝的同族元素,关于铊的下列性质判断中可能错误的是
A.是银白色质软的金属 B.形成+3价的化合物
C.T1(OH)3是两性氢氧化物 D.单质铊的还原性比单质铝强.
3.在元素周期表的金属和非金属的分界线的附近可以找到
A.半导体材料 B.人畜安全的高效农药
C.催化剂 D.氟利昂的代用品
2.现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,与钾元素同周期,则下列关于硒的叙述中不正确的是
A.原子序数为34 B.最高价氧化物的化学式为SeO3
C.非金属性比较强 D.气态氢化物化学式为H2Se
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com