
题目列表(包括答案和解析)
7、下列说法中正确的是
A、原子之间的强烈的相互作用叫化学键
B、离子键一定是金属离子和非金属离子之间通过静电作用形成的化学键
C、离子化合物也可能全部由非金属元素组成
D、两种非金属原子之间能形成离子键
6、可逆反应在一定条件下达到化学平衡状态的标志是
A.反应停止了 B.正反应速率与逆反应速率均为零
C.反应物和生成物浓度相等D.正反应速率与逆反应速率相等
5、元素性质呈周期性变化的决定因素是
A、元素原子半径大小呈周期性变化
B、元素相对原子质量依次递增
C、元素原子核外电子排布呈周期性变化
D、元素的最高正化合价呈周期性变化
4、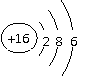 下列粒子的结构示意图中不正确的是
下列粒子的结构示意图中不正确的是
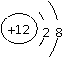
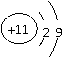
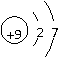
A、S B、F C、Na D、Mg2+
3、下列关于碱金属某些性质的排列,正确的是
A、电子层数:Li<Na<K<Rb<Cs
B、密度:Li<Na<K<Rb<Cs
C、熔、沸点:Li<Na<K<Rb<Cs
D、还原性:Li>Na>K>Rb>Cs
2、放射性同位素钬166 67Ho的原子核内中子数是
A、32 B、67 C、99 D、166
1、下列说法中正确的是
A、元素周期表中有七个横行,也是七个周期
B、元素周期表有九个横行,分为九个周期
C、元素周期表有十八个纵行,分为十八个族
D、元素周期表中第IA族元素都为金属元素
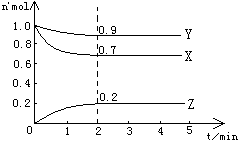
5.某温度时,在2L容器中X、Y、Z 三种物质的物质的量随时间的变化曲线如右图所示,由图中数据分析,该反应的化学方程式为
4.在100℃时,将0.100mol的四氧化二氮气体充入1L 抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
|
时间/s 浓度/mol·L-1 |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4)/mol·L-1 |
0.100 |
c1 |
0.050 |
c3 |
a |
b |
|
c(NO2)/?mol·L-1 |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为 ;达到平衡时四氧化二氮的转化率为 % ;
(2)20s时四氧化二氮的浓度 c1= mol·L-1,在 0s-20s内四氧化二氮的平均反应速率为 mol·(L·s)-1;
3、所示中a为生铁,A、B两个烧杯中为海水,C烧杯中为1mol·L-1的稀硫酸。
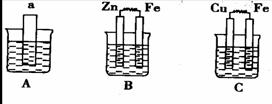 (1)C中Cu极的电极反应式为:
(1)C中Cu极的电极反应式为:
_________________。
(2)B中Zn极的电极反应式为:
______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com