
题目列表(包括答案和解析)
22.下表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
1 |
A |
|
||||||
|
2 |
|
|
|
D |
E |
J |
G |
|
|
3 |
B |
|
C |
J |
F |
|
H |
I |
(1) 表中元素,化学性质最不活泼的是 ,可用于制半导体材料的元素是_______。
(2) 最高价氧化物的水化物碱性最强的是 ,酸性最强的是 ;(填写最高价氧化物的水化物的化学式)
(3) A与E形成的化合物电子式是 。
(4)B单质与J的氢化物反应的化学方程式为
______________________________________________。
21、(1)在下列原子(或离子)结构简图上表示的微粒中(用元素符号填空)

①半径最小的是 ; ②具有最低负化合价的是 ;
③只有还原性的是 ;④只有氧化性的是 ;
(2)符号 1 1H、 2 1H、 3 1H、2312Mg、2412Mg和6529Cu表示的共有______种元素,_______种原子,中子数最多的粒子是___________。
(3)A元素的最高价为+5,其负价为 。B元素的最高价氧化物的化学式是B2O7,其氢化物的化学式为 。
(4)对主族元素而言,按要求填写下列空白。
①化合价主要决定于 。②同位素主要决定于 。
③质量数决定于 。④原子序数决定于 。
⑤元素的化学性质主要决定于 。
20、同周期的A、B、C三元素,其最高价氧化物对应水化物的酸性强弱顺序是:HAO4>H2BO4>H3CO4,则下列判断错误的是
A、原子半径A>B>C
B、气态氢化物稳定性HA>H2B>CH3
C、非金属性A>B>C
D、阴离子半径C3->B2->A-
19、重水a(D2O)和普通水b(H2O)分别是足量的金属钠反应,下列叙述正确的是
A、a、b质量相等时,产生气体的体积在同温、同压下相等
B、 a、b质量相等时,产生气体的质量相等
C、 a、b的物质的量相等时,产生气体的体积在同温、同压下相等
D、a、b的物质的量相等时,产生气体的质量相等
18.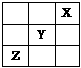 短周期元素X、Y、Z在周期表中的位置如右图所示,则下列说法正确的是( )
短周期元素X、Y、Z在周期表中的位置如右图所示,则下列说法正确的是( )
A.Z一定是活泼的金属
B.Y的最高价氧化物的水化物是一种强酸
C.Z的最高价氧化物的水化物是强酸
D.元素非金属性Z>Y
17.X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的
代数和为6,X和Y两元素形成的化合物为R,下列关于R的叙述正确的是( )
A.R 一定是共价化合物 B.R一定是离子化合物
C.R可能是共价化合物,也可能是离子化合物 D.R只能是气态物质,不可能是固态物质
16.某元素最高价氧化物对应水化物的化学式为H2XO3,这种元素的气态氢化物的化学式
可能是( )
A.HX B.H2X C.XH3 D.XH4
15、某元素的原子最外层有两个电子, 该元素 ( )
A.是ⅡA族元素 B.是金属元素
C.是稀有气体元素 D.无法确定属哪一类
14.下列事实,不能说明氯元素的非金属性比硫元素强的是:
A.氯气与H2S能发生置换反应 B.HClO4酸性比H2SO4强
C.盐酸是强酸,H2S是弱酸 D.受热时,氯化氢比硫化氢稳定
13.根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
A.铍的原子失电子能力比镁弱 B.砹的氢化物不稳定
C.H2Se比H2S稳定 D.NaOH比Mg(OH)2的碱性强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com