
题目列表(包括答案和解析)
39. 某有机物13.2g在过量的氧气中完全燃烧,把燃烧后的气体缓慢通过足量的碱石灰,碱石灰增重44.88g;若把燃烧后的气体通过浓硫酸,浓硫酸增重15.84g。已知该有机物的蒸气密度是相同条件下氢气的30倍。通过计算写出该有机物的分子式。
吉林毓文中学2009-2010学年度下学期期中考试
37.有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数两倍,C燃烧时呈现黄色火焰,C的单质在加热条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物E,试根据以上叙述回答:
(1)元素名称:A ________ B __________ C __________ D
___________;
(2)化合物E中含有的化学键类型为____
________;
(3)用电子式表示化合物 C2D 的形成过程_____________ ________________。
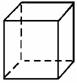 38.“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示:则立方烷的分子式为________。二氯代立方烷有 种。
三.计算题
38.“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示:则立方烷的分子式为________。二氯代立方烷有 种。
三.计算题
36.下表是元素周期表的一部分,针对表中的①-⑩种元素,填写下列空白。
 主族 主族周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
O |
|
2 |
|
|
|
① |
② |
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在这些元素中,化学性质最不活泼的是___ ___(填元素符号)这种原子的原子结构示意图为___ ____。
(2)用电子式表示元素⑦的单质分子的形成过程______ ___
(3)在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是___ _____(填化学式)。在金属元素氧化物所对应的水化物中,碱性最强的化合物是___ ____(填化学式),具有两性的化合物是___ _ __ _(填化学式)。
(4)地壳中含量最多的元素是___ ___(填元素符号),空气中含量最多的元素是___ ___(填元素符号),常温下呈液态的非金属单质是_____ ____(填化学式)。
(5)元素③的氢化物的电子式为___ ____。元素③的氢化物分别跟元素⑦、元素⑨的单质反应的化学方程式是_______________________、
。
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
33.在恒温恒容的容器中进行反应 A(g)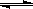 2B(g)+C(g),若反应物浓度由0.1mol·L-1降到0.06mol·L-1需20s,那么由0.06mol·L-1降到0.024mol·L-1,需反应的时间为( )
A.等于18s B.等于12s C.大于18s D.小于18s
34.下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快的是( )
A.V(H2)==0.1 mol/(L·min) B.V(N2)==0.1mol/(L·min)
C.V(NH3)==0.15mol/(L·min)
D.V(N2)==0.002mol/(L·s)
35.右图是可逆反应X2 + 3Y2
2B(g)+C(g),若反应物浓度由0.1mol·L-1降到0.06mol·L-1需20s,那么由0.06mol·L-1降到0.024mol·L-1,需反应的时间为( )
A.等于18s B.等于12s C.大于18s D.小于18s
34.下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快的是( )
A.V(H2)==0.1 mol/(L·min) B.V(N2)==0.1mol/(L·min)
C.V(NH3)==0.15mol/(L·min)
D.V(N2)==0.002mol/(L·s)
35.右图是可逆反应X2 + 3Y2 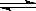 2Z2 在反应过程中的反应速率(v)与时
2Z2 在反应过程中的反应速率(v)与时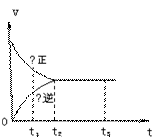 间(t)的关系曲线,下列叙述正确的是( )
A.t1时,只有正方向反应
B.t2时,反应到达限度
C.t2- t3,反应不再发生
D.t2- t3,各物质的浓度相等
间(t)的关系曲线,下列叙述正确的是( )
A.t1时,只有正方向反应
B.t2时,反应到达限度
C.t2- t3,反应不再发生
D.t2- t3,各物质的浓度相等
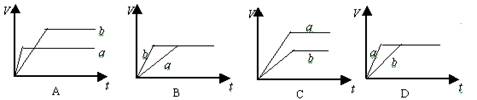
32.等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是 ( )
31.在盛有稀 H2SO4 的烧杯中放入用导线连接锌片和铜片,下列叙述正确的是( )
A.正极附近的 SO4 2- 离子浓度逐渐增大 B.电子通过导线由铜片流向锌片
C.溶液的pH逐渐变小 D.铜片上有 H2 逸出
30.下列物质中只有离子键的是
A.Cl2 B.NaOH C.MgCl2 D.H2O
29.上个世纪80年代,科学家通过研制发现了一种新分子,其化学式是C60。有关C60的下列说法中不正确的是( )
A、C60中可能含有离子键 B、C60中的化学键只有共价键
C、C60的一个分子中有60个碳原子 D、C60是由碳元素组成的单质
27.将1mol N2和3 mol H2通入4L的密闭容器中反应,半分钟后测得H2的物质的量为2.1 mol,现用如下三种物质在单位时间内的浓度变化来表示该反应速率:①v(N2) = 0.15 mol/(L·min) ②v(N2) = 1.05 mol/(L·min) ③v(NH3) = 0.30 mol/(L·min)其中正确的是( ) A.①② B.②③ C.①③ D.①②③ 28.从化学键的角度看化学反应的实质是“旧化学键的断裂,新化学键的形成”,下列既有旧化学键的断裂,又有新化学键的形成的变化是( )
A.酒精溶解于水 B.碘升华
C.氯化钠受热熔化 D.Cl2溶于水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com