
题目列表(包括答案和解析)
19.(6分)在原子序数为1─18号元素中,与水反应最剧烈的金属元素是______;化学方程式为__________________________________。与水反应最剧烈的非金属元素是_______;化学方程式为__________________________________。其中第三周期中,原子半径最大的金属元素是________; 元素的最高价氧化物所对应的酸最强的是________。高*考*资*源*网
18.只用一种试剂就能将Na2SiO3、Na2CO3、MgCl2、Ba(HCO3)2四种无色溶液区别开来,这种试剂是 ( )
A.氢氧化钠溶液 B.澄清石灰水 C.2 mol / L 盐酸 D.2 mol / L 硫酸

16.下列离子方程式正确的是 ( )
A.向石灰石中加稀硫酸 CaCO3+2H+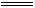 Ca2++H2O+CO2
Ca2++H2O+CO2
B.向澄清石灰水中通入过量二氧化碳Ca(OH)2+2CO2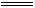 Ca2++2HCO3
Ca2++2HCO3
C.氯化氢通过饱和小苏打溶液 HCO3-+H+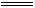 H2O+CO2
H2O+CO2
D.向碳酸氢钙溶液中加入足量烧碱溶液 Ca2++HCO3-+OH- 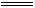 CaCO3¯+H2O 17.两种金属的碳酸盐或酸式碳酸盐的混合物50.0 g与足量的稀盐酸反应,标准状况下收集
CaCO3¯+H2O 17.两种金属的碳酸盐或酸式碳酸盐的混合物50.0 g与足量的稀盐酸反应,标准状况下收集
到CO2气体11.2 L,则此混合物的组成可能为 ( )
A.NaHCO3和KHCO3 B.Na2CO3和Li2CO3高*考*资*源*网
C.Ca(HCO3)2和CaCO3
D.NaHCO3和MgCO3

 w_w w. k#s5_
w_w w. k#s5_
15.将下列物质的量浓度相等的溶液等体积混合后(两两混合)有白色沉淀生成,加入过量的稀HNO3后,沉淀消失并放出气体,再加AgNO3溶液又有白色沉淀生成的是 ( )
A.Na2CO3和Ca(OH)2 B.Na2CO3和CaCl2
C.Na2SiO3和HCl
D.Ca(HCO3)2和NaOH

 w_w w. k#s5_
w_w w. k#s5_
14.下列叙述正确的是 ( )
A.非金属原子间以共价键结合的物质都是共价化合物

 w_w w. k#s5_
w_w w. k#s5_
B.含有共价键的化合物都是共价化合物
C.凡是能电离出离子的化合物都是离子化合物
D.凡是含有离子键的化合物都是离子化合物高*考*资*源*网
13.关于SO2和SO3的说法错误的是:①都是酸酐,②与水化合都能生成相应的酸,③都能与碱反应生成正盐或酸式盐,④通常条件下都是气体,⑤都能由硫单质与氧气直接化合制得 ( )
A.①④ B.④⑤ C.③⑤ D.②③
12. 同周期的X、Y、Z三元素,它们最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4 ,则下列判断正确的是 ( )
A.含氧酸的酸性H3ZO4>H2YO4>HXO4,

 w_w w. k#s5_
w_w w. k#s5_
B.非金属性X <Y<Z
C.元素的最低负化合价的绝对值按X、Y、Z变大
D.气态氢化物的稳定性按X、Y、Z的顺序增强
11. 将x mo1 Na2SO3和y mo1 Na2S完全溶于水后,再加入稀H2SO4酸化,其产物可能有三
种情况:① 生成物只有S、Na2SO4和水;② 生成物为SO2、S、Na2SO4和水;③ 生成物为H2S、S、Na2SO4和水。则x∶y的值也应有三种情况:a(大于0.5),b(小于0.5),c(等于0.5),按上述①、②、③顺序选出x∶y的值排列正确的是 ( )
A.c、a、b B. a、b、c C. a、c、b D.c、b 、a
10.0.05 mol某金属单质与足量的盐酸反应,放出1.12 L H2(标准状况),并转变为具有Ar原子的电子层结构的离子,该金属元素在元素周期表中的位置是 ( )
A.第三周期第IA族 B.第四周期第IA族高*考*资*源*网
C.第三周期第ⅡA族
D.第四周期第ⅡA族

 w_w w. k#s5_
w_w w. k#s5_
9.已知:①硫酸比氯酸稳定;②硫酸的酸性弱于高氯酸;③H2S比HCl易被氧化;④HCl
比H2S更容易由单质合成;⑤盐酸的酸性比H2S的酸性强。上述事实能够说明硫的非金属性比氯弱的是 ( )
A.①②③ B.③④⑤ C.②③④ D.①③⑤

 w_w w. k#s5_
w_w w. k#s5_
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com