
题目列表(包括答案和解析)
26. (8分)实验室可用右图所示装置(缺少收集装置)制备并收集氨气。
(8分)实验室可用右图所示装置(缺少收集装置)制备并收集氨气。
(1)写出试管A中发生反应的化学方程式: 。
(2)在图中绘出用试管收集氨气的仪器装置简图。
(3)要检验氨气是否收集满,方法是 。w_w w.k_s 5*
(4)若将224体积(标准状况)的氨气溶解在1体积水中,所得氨水密度为0.93 g/cm3,则该氨水的物质的量浓度是 (计算结果保留2位小数)。
25.(8分)A-H 8种物质的转化关系如下图所示(部分生成物略去)。化合物B中阴阳离子数目之比为2∶1,C是无色有刺激性气味的气体,C、D的分子均为10电子微粒。w_w w.k_s 5*
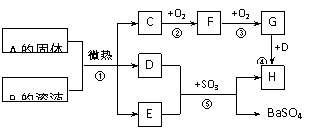
请回答下列问题:

 w_w w. k#s5_
w_w w. k#s5_
(1)写出F、H的化学式:F ,H 。
(2)反应①的离子方程式为 ,反应②的化学方程式是 。
(3)在反应①-⑤中,属于氧化还原反应的是 。w_w w.k_s 5*
24.(6分)Q、R、X、Y、Z为短周期元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,R与Y原子的价电子数之比为2∶3,Y和Z的阴离子与Ar原子的电子层结构相同且Y的原子序数小于Z。

 w_w w. k#s5_
w_w w. k#s5_
(1)工业上用Q单质与R的氧化物制备单质R,反应的化学方程式是 。
(2)R的氢化物分子空间构型是正四面体,属于________分子(填“极性”或“非极性”);R与X形成的化合物可作为一种重要的高温结构陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是_____________。w_w w.k_s 5*
(4)Y与Z可形成极性分子YZ2,该分子的电子式是________________。
23.(6分)下表的实线是元素周期表部分边界。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
…… |
(1)请在表中用实线补全元素周期表的边界。在表中标出第4周期位于金属与非金属分界线左右两侧的元素的符号。w_w w.k_s 5*
(2)元素周期表中非金属性最强的元素是 。第3周期元素中,其氧化物既能与盐酸作用,又能与NaOH溶液反应,该元素的原子结构示意图是 。
22. 已知,反应3Cl2+8NH3===N2+6NH4Cl在常温下很容易进行,化工厂可利用浓氨水检查氯气管道是否漏气。下列说法不正确的是

 w_w w. k#s5_
w_w w. k#s5_
A. 若管道漏气遇氨就会产生白烟 B. 该反应利用了Cl2的强氧化性
C. 该反应属于复分解反应 D. 生成1 mol N2有6 mol电子转移w_w w.k_s 5*
第Ⅱ卷(非选择题,共50分)
21. X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期,X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列说法正确的是
A. 元素非金属性由弱到强的顺序为Z<Y<X
B. Y元素最高价氧化物对应水化物的化学式可表示为H3YO4w_w w.k_s 5*
C. 3种元素的气态氢化物中,Z的气态氢化物最稳定
D. 原子半径由大到小的顺序为Y>Z>X
20. 门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是

 w_w w. k#s5_
w_w w. k#s5_
 A.X在高温下能与O2反应
B.XO2可被碳或氢气还原为Xw_w w.k_s 5*
A.X在高温下能与O2反应
B.XO2可被碳或氢气还原为Xw_w w.k_s 5*
 C.X的主要化合价为+2、+4价 D.X的单质不能与NaOH溶液反应放出H2
C.X的主要化合价为+2、+4价 D.X的单质不能与NaOH溶液反应放出H2
19. 下列离方程式书写正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.亚硫酸钡溶于盐酸:SO2-3 +2H+=== SO2↑+H2O
B.NH4HCO3溶液与足量NaOH溶液混合加热:
NH+4+HCO-3+2OH-△==== NH3↑+CO2-3 +2H2O
C.铜与浓硝酸反应:Cu+2H++NO-3===Cu2++NO2↑+H2O
D.SO2气体通入氯水中:SO2+H2O+Cl2=== HSO-3+2Cl-+H+w_w w.k_s 5*
18. 下列各组离子,在溶液中能大量共存,加入NaOH溶液后加热,既有气体放出又有沉淀生成的一组是
A.Ba2+、NO-3、NH+4、Cl- B.Ca2+、HCO-3、NH+4、SO2-4
C.Cu2+、HSO-3、K+、CO2-3 D.Mg2+、NH+4、SO2-4 、Cl-w_w w.k_s 5*
17. 已知1-18号元素的离子aW2+、bX+、cY2-、dZ- 都具有相同的电子层结构,下列关系正确的是

 w_w w. k#s5_
w_w w. k#s5_
A. 核电荷数数c>b B. 离子的还原性Z->Y2-w_w w.k_s 5*
C. 氢氧化物的碱性XOH>W(OH)2 D. 原子半径X<W
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com