
题目列表(包括答案和解析)
22、(8分)(1)氟; 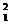 H ;
H ; 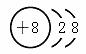 ; 共价键(极性键) (各1分)
; 共价键(极性键) (各1分)
(2)N2+O2
 2NO (2分)
2NO (2分)
(3)2Na+2H2O=2Na++2OH-+H2↑ (2分)
21、(12分)(1)正四面体形 (2分)
(2)强 (2分)
(3) (2分)
(2分)
(4)减小 (2分)
(5) (2分)
26.(10分)写出下列反应的化学方程式:
(1)工业上用氮气和氢气合成氨: 。
(2)金属铜与浓硝酸反应: 。
(3)氢氧化铝与氢氧化钠溶液反应: 。
(4)将二氧化硫气体通入氯水中: 。
(5)碳酸氢钠受热分解: 。
(6)苯与液溴在铁催化作用下反应: 。
(7)酒精在空气中点燃: 。
(8)溴乙烷与热的氢氧化钠水溶液反应: 。
(9)苯酚与溴水反应: 。
(10)将二氧化碳通入苯酚钠溶液中: 。
南安一中209-10学年高一下学期期末考试
化 学 试 卷 评 分 标 准
选择题(本题共有20小题,每小题2分,共40分。)
25.(12分) 经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一
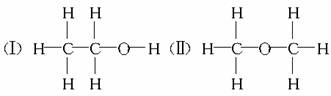
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙两位同学直接利用如图给定装置开始进行实验确定乙醇的结构
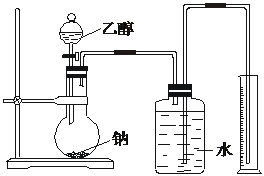
(1) 学生甲得到一组实验数据如上表:
|
乙醇的物质的量/mol |
氢气的体积/L |
|
0.10 |
1.12(标准状况) |
根据以上数据推断乙醇的结构为 (用Ⅰ、Ⅱ表示),理由为
,
该反应的化学方程式为: 。
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗? (填“正确”或“不正确”)。请说明你判断的理由

(3)实验后,两名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是 n(填“大于”、“小于”或“等于”)。
24.(8分)从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:
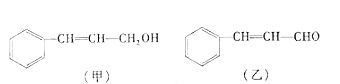
(1)甲中含氧官能团的名称为 ,乙中含氧官能团的名称为 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
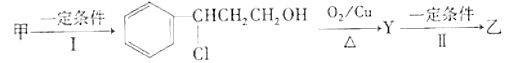
其中反应Ⅰ的反应类型为 ,反应Ⅱ的化学方程式为:
(注明反应条件)。
23.(10分)(1)在一定条件下制备氯乙烷(C2H5Cl),试回答:
①用乙烷制备氯乙烷的化学方程式是 ,
该反应的类型是 
②用乙烯制备氯乙烷的化学方程式是 ,
该反应的类型是 。
比较上述两种方法,第 种(填“①”或“②”)方法更好。
(2)聚乙烯塑料是由石油裂解产物乙烯通过加聚反应制得,写出乙烯反应生成聚乙烯的化学方程式 。
该反应的类型是 。
22.(8分)有A、B、C、D、E五种元素,它们可能是原子或离子,且均为短周期元素,A与B可形成BA型化合物,且A是非金属性最强的元素。金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍。D的气态氢化物水溶液显碱性,而其最高价氧化物水化物为强酸。E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个。
(1)写出A元素名称:______ _____;
C2粒子的符号:_____ _ _____;
画出E离子的结构示意图:______ ________;
A与C形成的化合物所含的化学键类型是:_____ ______。
(2)写出D单质与E单质化合反应的化学方程式:___________ __________。
(3)写出B的单质与水反应的溶液混合后发生的反应的离子方程式:
__________ _____。
21.(12分)下表是元素周期表的一部分,针对表中的①~⑧元素,填写下列空白:
|
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
① |
|
② |
|
|
|
3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
|
⑧ |
|
(1)①的气态氢化物分子的空间构型为__________ ________。^S*5U.C#O%下标
(2)②的气态氢化物稳定性比⑦的气态氢化物________(填“强”、“弱”或“相同”)。
(3)由①与②形成的三原子分子的电子式为_________ ___ __________。
由③与⑧形成的离子化合物的电子式为__________ __________。
(4)③、④、⑤离子半径依次_______ ___。(填“增大”、“减小”或“不变”)
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
。
20.由乙烯和乙醛组成的混合气体经测定,其中C的质量分数为72%,则混合气体中氧元素的质量分数为( )。
A.22% B.32% C.16% D.2%
选择题答案必须填写在答题卡上!
 南安一中2009-2010学年度高一下学期期末考试
南安一中2009-2010学年度高一下学期期末考试
化学试卷 答题卡 总分:
把第Ⅰ卷答案写在下列表格中(每小题2分,共40分)
第Ⅱ卷(非选择题,共60分)
19.为了除去苯中混有的少量苯酚,下面的实验正确的是( )。
A.在分液漏斗中,加入足量2mol·L-1NaOH溶液,充分振荡后,分液分离
B.在分液漏斗中,加入足量2mol·L-1FeCl3溶液,充分振荡后,分液分离
C.在烧杯中,加入足量的浓溴水,充分搅拌后,过滤分离 ^S*5U.C#O%下标
D.在烧杯中,加入足量冷水,充分搅拌后,过滤分离
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com