
题目列表(包括答案和解析)
72.下列关于铜-锌-稀硫酸构成的原电池的有关叙述,错误的是( )
A.锌为负极,锌发生氧化反应
B.铜为正极,铜不易失去电子而收到保护
C.负极发生还原反应,正极发生氧化反应
D.外电路电子流入的一极为正极,电子流出的一极为负极
71.按照下述实验制备气体,合理而又实用的是( )
A. 锌粒和稀硝酸反应制备氢气
B. 大理石和浓硫酸反应制备二氧化碳
C. 二氧化锰和稀盐酸加热制备氯气
D. 向浓盐酸中滴加浓硫酸制备氯化氢气体
70. 表明金属甲的活动性比金属乙的活动性强的叙述正确的是 ( )
A.在氧化还原反应中,甲失电子比乙失电子多
B.甲比乙同价态阳离子的氧化性强
C.甲能与稀盐酸反应生成氢气而乙不能
D.将甲、乙组成原电池时,甲为负极
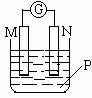
69. 下图所示装置中,可观察到电流计指针偏转,M棒变粗,N棒变细,下表所列M、N、P物质中,可以组合成该装置的是 ( )
|
选项号 |
M |
N |
P |
||
|
A |
锌 |
铜 |
稀硫酸 |
||
|
B |
铜 |
铁 |
稀盐酸 |
||
|
C |
银 |
锌 |
|
||
|
D |
锌 |
铁 |
硝酸铁溶液 |
68. 下图所示装置能够组成原电池,并且能产生明显电流的是( )

67.埋在地下的输油铸铁管道,在下列各种情况下,被腐蚀速度最慢的是( )
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多,潮湿透气的中性土壤中
66.下列各组实验中溶液最先变浑浊的是( )
A.0.1mol/LNa2S2O3溶液和0.1mol/L稀H2SO4、各5mL,另加蒸馏水5mL,反应温度10℃
B.0.1mol/L Na2S2O3溶液和0.1mol/L稀H2SO4各5mL,另加蒸馏水10mL,反应温度10℃
C.0.1mol/L Na2S2O3溶液和0.1mol/L稀H2SO4各5mL,另加蒸馏水10mL,反应温度30℃
D.0.2mol/L Na2S2O3溶液和0.2mol/L稀H2SO4各5mL,另加蒸馏水10mL,反应温度30℃
65.在一定温度下,可逆反应:A2(气)+B2(气)  2AB(气),达到平衡的标志是( )
2AB(气),达到平衡的标志是( )
A.容器的总压强不随时间而变化
B.单位时间内有nmol A2生成的同时有nmol B2生成
C.单位时间内有nmol B2发生反应的同时有nmol AB分解
D.单位时间内生成nmol A2同时就有2nmol AB生成
64.把下列4种x的水溶液,分别加进盛有10mL2mol/L盐酸的烧杯中,并加水稀释到50mL,问下列哪种x的溶液与盐酸的反应速率最大( )
A.20 mL 3mol/L B.20 mL 2 mol/L
C.10 mL 4 mol/L D.10 mL 2 mol/L
63.实验室可以用铁片与稀硫酸反应制取氢气,下列措施不能使氢气的生成速率增大的是( )
A.加热 B.不用稀硫酸,改用质量分数为98%的浓硫酸
C.不用铁片改用镁条 D.不用铁片,改用铁粉
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com