
题目列表(包括答案和解析)
21.现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
有三个电子层,K、M层电子数之和等于L层电子数 |
|
B |
短周期中金属性最强 |
|
C |
常温下单质为双原子分子,氢化物的水溶液呈碱性 |
|
D |
元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;
②B元素原子结构示意图 ;
③C单质分子的电子式 ;用电子式表示A和B元素组成的化合物的形成过程 ;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素 。
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是 (写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
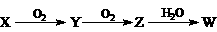
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为: ;生成该白色沉淀的化学方程式为 ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为: 。
20.验证某有机物中含有氧元素,应完成的实验内容是( )
A.只有验证它完全燃烧后产物只有H2O和CO2
B.测定该试样的质量及该试样完全燃烧后生成CO2和H2O的质量
C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比
D.只有测定其燃烧产物中H2O和CO2物质的量的比值
19.某有机物的结构简式如图所示,则该有机物不可能具有的性质是( )
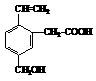 A.能跟NaOH溶液反应
B.能使酸性KMnO4溶液褪色
A.能跟NaOH溶液反应
B.能使酸性KMnO4溶液褪色
C.能发生酯化反应 D.能发生水解反应
18.下列有机物不能通过乙烯的加成反应制取的是( )
A.CH3CH2Cl B.CH2Cl-CH2Cl C.CH3-CH2OH D.CH3-COOH
17.不能用溴水鉴别的是( )
A.甲烷、乙烯 B.苯、乙醇 C.乙醇、乙酸 D.苯、四氯化碳
16.从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液的氧化性,催熟水果
D.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
15.在一定条件下,对于密闭容器中进行的可逆反应:N2 + 3H2 2NH3,下列说法中,能充分说明这一反应已经达到化学平衡状态的是( )
A.N2、H2与NH3的物质的量之比为1︰3︰2 B.N2、H2与NH3的浓度相等
C.各组分的浓度不再发生变化 D.反应停止,正、逆反应速率都等于零
14.反应4NH3(g)+5O2(g)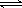 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率v (X)可表示为( )
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率v (X)可表示为( )
A.v (NO)=0.0010 mol·L-1·s-1 B.v (O2)=0.0010 mol·L-1·s-1
 C.v (NH3)=0.010
mol·L-1·s-1 D.v (H2O)=0.045 mol·L-1·s-1
C.v (NH3)=0.010
mol·L-1·s-1 D.v (H2O)=0.045 mol·L-1·s-1
13.下列各组实验中,过氧化氢分解最快的是( )
|
|
H2O2的浓度(质量分数) |
温度(℃) |
催化剂的使用 |
|
A |
2 |
10 |
使用MnO2 |
|
B |
4 |
10 |
不使用 |
|
C |
6 |
30 |
使用MnO2
|
|
D |
6 |
30 |
不使用 |
12.下列说法中不正确的是( )
A.化学反应中的能量变化,通常表现为热量的变化
B.反应物的总能量高于生成物的总能量时发生放热反应
C.Ba(OH)2·8H2O与NH4Cl的反应是吸热反应
D.木炭在氧气中的燃烧是吸热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com