
题目列表(包括答案和解析)
1.随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N5+等已被发现。下列有关说法中,正确的是 ( )
A.H2与H3属于同素异形体 B.O2与O4属于同位素
C.C60的质量数为 720g/mol D.N5+中含有36个电子
常用原子量: H:1 O:16 N:14 Si:28 Na:23 Cu:64 Mg:24 O:16 Cl:35.5 Fe:56
30.(10分)
从海水中可以获得淡水、食盐并可提取镁和溴等物质。
(1)海水淡化的方法主要有 (填一种)。
(2)经过化学变化才能从海水中获得的物质是 (填序号)
A.氯、溴、碘 B.钠、镁、铝 C.烧碱、氢气 D.食盐、淡水
(3)从海水中提取镁的流程如下图所示:
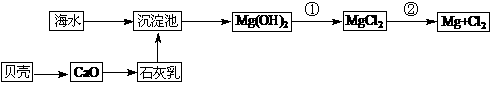
反应①的离子方程式为 。
反应②的化学方程式为 。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子
方程式为 。
29.(12分)
某化学研究性学习小组开展实验探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊, 持续通入发现浑浊又变澄清。由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:气体可能为CO2; 猜想2: ;
猜想3: 。
为了验证猜测,该小组设计实验加以探究:
[实验探究]该小组按如图所示装置,将气体从a端通入,则:

(1)B中应该装入下列 试剂(填编号)
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红的作用是: ;
(3)D中澄清石灰水的作用是: 。
通过该实验,小组同学观察到以下三个实验现象:
① A中品红褪色 ② C中品红不褪色 ③ D中澄清石灰水变浑浊
[得出结论]由上述现象小组同学确认该气体的成分是 。
28.(12分)
下表是某兴趣小组通过实验获得的稀硫酸与某金属反应的实验数据:
|
实验 序号 |
金属 质量/g |
金属 状态 |
c(H2SO4) mol/L |
V(H2SO4) mL |
溶液温度/℃ |
金属消失 的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
250 |
|
2 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
3 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
125 |
|
4 |
0.10 |
丝 |
1.0 |
50 |
35 |
50 |
50 |
分析上述数据,回答下列问题:
(1)上述反应中,反应物的总能量比生成物的总能量 (选填“高”、“低”或“相等”)。
(2)实验1、2可得出的结论是 ;
实验3、4可得出的结论是 。
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡。该金属的金属活动性比铁 (选填“强”或“弱”),铁电极上发生的电极反应式为 。
27.(12分)
2010年4月14日7时49分在青海省玉树地区发生7.1级地震,造成了重大的人员伤亡和财产损失。为了保证震区的卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。
回答下列问题:
(1)漂白液的有效成分是(填化学式) ;
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3-5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质 (填序号)。
A.酸性 B.碱性 C.强氧化性 D.还原性
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
。
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由 。
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3 +4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为 。
26.(14分)
下表为元素周期表的一部分,请参照①-⑩在表中的位置,用化学用语回答下列问题:
|
① |
|
|
|||||||||||||||
|
|
|
|
|
② |
③ |
④ |
⑤ |
|
|||||||||
|
⑥ |
|
⑦ |
|
|
⑧ |
⑨ |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑩ |
|
|
|
|
(1)元素③形成的单质的电子式为 ;元素②形成的最高价氧化物的结构式为 。
(2)⑥、⑦两元素的最高价氧化物的水化物之间反应的离子方程式为 。
(3)②、③、④、⑤元素形成的氢化物中,热稳定性最强的是 (填化学式),沸点最高的是 (填化学式)。
(4)⑧、⑨元素的最高价氧化物的水化物酸性强弱比较 > (填化学式)。
(5)用电子式表示⑥、⑧两元素结合成化合物的形成过程 。
(6)元素⑩在周期表中的位置 ;该元素的单质主要用途 (填一种)。
25.传统的硅酸盐工业产品有:玻璃、水泥、陶瓷。在实验室进行物质分离提纯操作实验时,使用的实验仪器大多属于硅酸盐质仪器。下列实验仪器属于硅酸盐质的是
A.蒸发皿 B.石英坩埚 C.三脚架 D.分液漏斗
增城市2010学年度第二学期期末统考试卷
高一化学
第Ⅱ卷(选择题共60分)
24.短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y 与Z
与Z 核外电子层的结构相同。下列化合物中同时存在离子键和共价键的是
核外电子层的结构相同。下列化合物中同时存在离子键和共价键的是
A.Z2Y B.Z2Y2 C.X2Y2 D.ZYX
23.对下列实验现象的解释正确的是
|
选项 |
实验现象 |
解释 |
|
A |
Cl2使鲜艳的红色花瓣褪色 |
Cl2具有漂白性 |
|
B |
NH3与HCl气体接触时有白烟产生 |
NH3与HCl反应生成NH4C1固体小颗粒 |
|
C |
冷浓硝酸可以用铝罐贮存 |
浓硝酸使金属铝发生钝化 |
|
D |
SO2使氢氧化钠的酚酞溶液褪色 |
SO2具有酸性 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com