
题目列表(包括答案和解析)
1.关于化学能与热能的叙述,正确的是
A.1mol酸与碱恰好中和时所放出的热量叫中和热
B.化学反应中的能量变化,主要是由化学键变化引起的
C.需要加热才能发生的反应,一定是吸热反应
D.反应物的总能量高于生成物总能量的反应,不需要加热就可自行反应
21. (10分)
(1)将镁条投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是 ,一定时间后反应速率逐渐减慢,其原因是 。
(2)用铂电极放置在KOH溶液中,然后向两极分别通入CH4和O2即可发电(为燃料电池)。负极的电极反应式为CH4+10OH--8e→CO32 - +7H2O,则正极的电极反应式为___________,放电时溶液中的阴离子向_________移动(填“正极”或“负极”) 。
(3)分子式为C4H10O,能和金属钠反应放出H2的同分异构体有 种。
当涂一中2009-2010学年度第二学期期末考试
20.(10分)
工业上从海水中提取溴的方法如下:
①将蒸馏(制淡水)后浓缩的海水用硫酸进行酸化;
②向酸化的海水中通入足量氯气,使溴离子转化为溴单质;
③向上述溶液中通入空气和水蒸气,将溴单质吹入盛有二氧化硫水溶液的吸收塔内转化成氢溴酸;
④向吸收塔内通入适量的氯气;
⑤用四氯化碳萃取吸收塔中的溴单质。
请完成下列问题:
(1)在实验室中蒸馏海水制淡水时,常用的仪器除了酒精灯、锥形瓶、牛角管、冷凝管、石棉网及必要的夹持仪器,还需要的玻璃仪器有 ;蒸馏时碎瓷片的作用是__________________________。
(2)步骤②中反应的离子方程式为
(3)步骤③的目的是使溴单质富集,试写出溴单质与二氧化硫水溶液反应的化学方程式
。
(4)下列能代替四氯化碳来萃取溴的试剂是 (填序号)
A.盐酸 B.酒精 C.乙酸 D.苯
19.(8分)
苯的特殊结构决定苯的特殊性质。
(1)苯 使酸性高锰酸钾溶液褪色(填“不能”、能”);把约2 ml苯滴入10 ml溴水中充分振荡后静置,出现的现象是:
(2)苯既能发生加成反应又能发生取代反应,由苯生成硝基苯的化学方程式为:
(3)苯与H2发生加成反应的化学方程式为:
18.(12分)
有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20;X、Z是金属元素;V和Z元素原子的最外层电子都只有一个;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可知:
(1)X在元素周期表中的位置是 ,其最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应反应的离子方程式为
(2)W和Y对应的氢化物的稳定性大小关系是 (用化学式表示),形成Z元素最高价氧化物对应水化物的化学键类型是
(3)V与W形成原子个数之比为1:1的化合物的电子式为
(4)工业制取X单质的化学方程式为
17.(12分)
已知乙烯能发生以下转化关系:
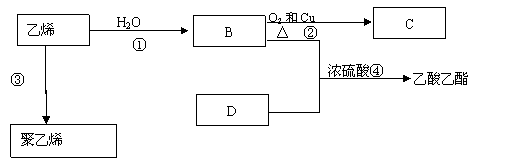
试回答下列问题:
(1)D中官能团名称 ,反应④的反应类型
(2)写出反应的化学方程式
①:
②:
③:
④:
16.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法正确的是 ( )
A.混合气体中一定有甲烷
B.混合气体中一定是甲烷和乙烯
C.混合气体中可能有乙烷
D.混合气体中一定有乙炔(CH≡CH)
15.下列分子的所有原子都在同一平面上的是( )
A.H2C===CHCl B.甲苯
C. H2C===CHCH3 D.乙烷
14.下列属于加成反应的是( )
A. 己烯使酸性高锰酸钾溶液褪色
B. 将苯滴入溴水中,振荡后水层接近无色
C. 乙烯使溴水褪色
D. 甲烷与氯气混合光照一段时间后黄绿色消失
13.在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol·L-1,则在这10 min内NH3的平均反应速率是 ( )
A、0.1 mol·L-1·min-1 B、0.2 mol·L-1·min-1
C、0.3 mol·L-1·min-1n-1 D、0.6 mol·L-1·min-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com