
题目列表(包括答案和解析)
1.下列生活里常见现象中,一定涉及化学变化的是
A.冰雪融化 B.美酒飘香 C.点燃蜡烛 D.榨取果汁
21.(16分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)实验室中现有 、
、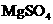 、
、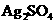 、
、 等4中溶液,可与实验中
等4中溶液,可与实验中 溶液起相似作用的是
;
溶液起相似作用的是
;
(4)要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
|
实验 混合溶液 |
A |
B |
C |
D |
E |
F |
|
4mol/LH2SO4/mL |
30 |
V1 |
V2 |
V3 |
V4 |
V5 |
|
饱和CuSO4溶液/mL |
0{ 007} |
0.5 |
2.5 |
5 |
V6 |
20 |
|
H2O/mL |
V7 |
V8 |
V9 |
V10 |
10 |
0 |
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
。
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
。
20.(18分)化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
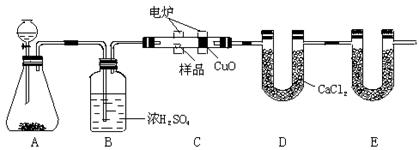
回答下列问题:
(1)A装置中分液漏斗盛放的物质是 ,写出有关反应的化学方程式: 。
(2)C装置(燃烧管)中CuO的作用是 。
(3)写出E装置中所盛放物质的名称 ,它的作用是 。
(4)若准确称取1.20g样品(只含C、H、O三种元素中的两种或三种)。经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的最简式为 。
20.混合气体的密度不再改变的状态 ( )
A.①④ B.②③⑤
C.①③④ D.①②③④⑤
第II卷 非选择题(2小题,共34分)
19.可逆反应:2NO2(g)  2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是 ( )
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是 ( )
A.单位时间内生成nmol O2的同时生成2nmol NO2
B.单位时间内生成nmol O2的同时生成2nmol NO
C.用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
D.混合气体的颜色不再改变的状态
18.下列描述的元素中,一定属于主族元素的有 ( )
A.元素的原子最外层电子个数为2
B.元素的原子最外层电子个数为6
C.位于元素周期表中ⅡA族右边的元素
D.阴离子RO4-中R元素
17.1 mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是 ( )

16.北京奥运会 “祥云”火炬所用燃料为丙烷,下列有关丙烷叙述中不正确的是 ( )
A.比甲烷的沸点高 B.与乙烷互为同系物
C.分子中的碳原子不在一条直线上 D.可发生加成反应
15. (21分) “酒是陈的香”,就是因为酒在储存过程中生成了有香 味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。
(21分) “酒是陈的香”,就是因为酒在储存过程中生成了有香 味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式
。
(2)饱和碳酸钠溶液的主要作用是
、 、 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上, 不能插入溶液中,目的是 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
选考部分
第I卷 选择题(每小题只有一个选项符合题意,共16分)
14.(10分)苯是一种重要的化工原料,也是一种重要的溶剂。请回答下列问题:
⑴把苯加入到盛有溴水的试管中,液体会出现分层现象,充分振荡、静置,出现橙红色液体的一层在 层(填“上”或“下”);
⑵把苯加入到盛有少量高锰酸钾溶液的试管中,振荡后,酸性高锰酸钾溶液不褪色,说明苯分子中 (填“有”或“没有”)碳碳双键;
⑶在浓硫酸作用下,苯在50-60℃可以与浓硝酸反应生成硝基苯,反应的化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com