
题目列表(包括答案和解析)
21(10分). (1) __________________________________。
(2)___________________。 _______________________________________________________。
(3) ___________________________(写化学式)(4) ____________。___ __________ 。
22(6分). (1) ______________________________________;
(2) ___________________________________;(3)______________________________________。
23(12分).
(1) 。(2) 。
(3) , 。
(4) 。 (5) 。
24(10分).(1)C , E ;
(2)①A→B: ; ;
②D+B→E: ; 。
|
座位号 |
|
26(6分).已知:氧化性强弱:Cl2>Br2>Fe3+;还原性强弱:Fe2+>Br->Cl-;
(1)下列反应能够发生的是: (可多选)
A.Cl2+2Fe2+→2Cl-+2Fe3+ B.2Cl-+Br2→Cl2+2Br-
C.Br2+2Fe2+→2Br-+2Fe3+ D.2Fe3++2Br-→2Fe2++Br2
(2)把少量的氯气通入FeBr2溶液中时,氯气可以氧化Fe2+和Br-,请问氯气先氧化哪一种离子? (填写离子符号)。
(3)往250mLFeBr2溶液中通入8.96L(标准状况)Cl2,反应完成后,溶液中1/2的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为多少?
27(6分).某有机物完全燃烧时只生成二氧化碳与水,取2.3g 该有机物完全燃烧,将产物通过浓硫酸,浓硫酸增重2.7g,继续将产物通过碱石灰,碱石灰增重4.4克,已知该有机物分子量 为46。
(1)求该有机物的分子式;
(2)写出该有机物可能的同分异构体的结构简式。
附加题:(本题包括2小题,每小题10分,共20分)
1(10分).向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

(2)整个过程中的还原剂有 。
(3)把KI换成KBr,则CCl4层变为____________色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为20mg-50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若庄Kl与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
2(10分).羧酸A和醇B(A、B中均只有一个官能团)形成的酯C,已知:①2.2g C燃烧可生成4.4gCO2和1.8g H2O;②1.76g C与50mL 0.5 mol. L-1的NaOH溶液共热后,为了中和剩余的碱液,耗去0.2 mol. L-1的盐酸25mL;③取C水解后所得的醇B 0.64g,跟足量的钠反应时,标况下收集到224mL H2。求:
(1)C的相对分子质量、分子式、结构简式。
(2)写出C与 NaOH共热反应的化学方程式:
 安吉县2010年高二夏令营活动统一抽测化学答题卷
安吉县2010年高二夏令营活动统一抽测化学答题卷
25(10分).某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
 [实验一]用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
[实验一]用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
(1)该反应的化学方程式为 ;(只写第一步)
(2)水槽中盛放的液体最好为 ;(填标号)
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
[实验二]用排蒸馏水法收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(3)该实验设计的错误之处 ;
[实验三]步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL 蒸馏水,充分振荡,测得pH =1.00。
(4)判断该反应中有氯化氢生成的依据是 ;
(5)假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00 mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为 mL。
21(10分).A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。1g A的单质与C的单质完全反应生成Y(Y为液态),放出142.9KJ的热量,请写出该反应的热化学方程式_______________________。
(3)若E的单质是常见的半导体材料,则A与B形成的常见化合物R、C与D形成的常见化合物S、C与E 形成的常见化合物T, R、S、T三者的沸点从高到低排列为____________(写化学式)
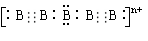 (4)画出B单质的结构式_______。最近科学家合成出了B元素形成的B
(4)画出B单质的结构式_______。最近科学家合成出了B元素形成的B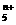 电子式
, 则n值为___ 。
电子式
, 则n值为___ 。
 22(6分).某溶液A可能含有Cu2+、NH4+、Al3+、Mg2+、Na+、Fe3+、SO42-中的几种。若取A溶液加固体Na2O2,有无色无味气体放出,并生成白色沉淀,加入Na2O2的量x与生成沉淀的量y用图表示。问:
22(6分).某溶液A可能含有Cu2+、NH4+、Al3+、Mg2+、Na+、Fe3+、SO42-中的几种。若取A溶液加固体Na2O2,有无色无味气体放出,并生成白色沉淀,加入Na2O2的量x与生成沉淀的量y用图表示。问:
(1) A中一定存在的离子有:______________________________________;
(2) A中一定不存在的离子有:___________________________________;
(3)当x=a时,写出所得溶液里溶质的电离方程式:_______________________。
 23(12分).A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品)。
23(12分).A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品)。
(1)若A为Na,B为NaOH,C为Na2CO3,请写出A转化为B的离子方程式 。
(2)若B为Al2O3,C为钠盐,试写出B转化为C的化学方程式 。
(3)若A为气态单质,B为漂白粉的主要成份之一,C具有漂白性。试写A转化为B的化学方程式 。画出组成单质A的元素原子结构示意图 。
(4)若A、B、C均为钠盐的水溶液,B转化为C是海水中提取溴的原理,请写出B转化为C的离子方程式 。
(5)若A常温下为固态单质,化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,且D、E为同一物质,则B为 。
24(10分).气态烃A在催化剂作用下加压、加热与水反应制得B,B在一定条件下氧化可得C,C在催化剂作用下与氧气反应可得D,D和B与浓硫酸混合加热可得到有香味的无色油状液体E。它们的转化关系如下:

请回答下列问题:
(1)推断下列物质: C , E ;
(2)写出下列反应方程式并指出反应类型。
①A→B: ;属 反应;
②D+B→E: ;属 反应;
20.向Fe2(SO4)3、CuCl2混和溶液中投入足量的铁粉充分反应后,得到的固体经过滤、干燥、称重,知所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比是
A.3︰2 B.1︰7 C.2︰7 D.3︰14
19.一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶3 B.5∶4 C.1∶1 D.3∶5
18.下图为元素周期表前四周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法正确的是
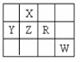 A.五种元素的原子最外层电子数一定大于2 B.五种元素一定都是非金属元素
A.五种元素的原子最外层电子数一定大于2 B.五种元素一定都是非金属元素
C.R的最高价氧化物对应的水化物一定是强酸 D.Y的氧化物一定具有两性
17.下列关于有机物的说法中正确的是:①棉花、蚕丝和人造丝的主要成分都是纤维素 ②淀粉、油脂、蛋白质在一定条件下都能发生水解 ③有机物完全燃烧后都只能生成二氧化碳和水 ④除去乙酸乙酯中残留的乙酸,加过量饱和Na2 CO3溶液振荡后静置分液 ⑤塑料、橡胶和光导纤维都是合成高分子材料 ⑥石油的分馏、裂化和煤的干馏都是化学变化
A.①⑤⑥ B.②④ C.①②③⑤ D.③④⑤⑥
16.已知反应X + Y = M + N为吸热反应,对这个反应的下列说法中正确的是
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com