
题目列表(包括答案和解析)
4.下列叙述中能肯定说明金属A比金属B的活泼性强的是 ( )
A.常温时,A能从酸中置换出氢,而B不能
B.A原子电子层数比B原子的电子层数多
C.1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多
D. A原子最外层电子数比B原子的最外层电子数少
5 .用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是: ( )
A.不用稀硫酸,改用98%浓硫酸 B.加热
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
6 一定温度下,反应N2(g)+3H2(g)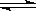 2NH3(g)达到化学平衡状态的标志是: ( )
2NH3(g)达到化学平衡状态的标志是: ( )
A.N2,H2和NH3的物质的量分数不再改变
2)∶c(H2)∶c(NH3)=1∶3∶2
C.N2与H2的物质的量之和是NH3的物质的量2倍
D N2,H2和NH3的分子个数之比为1∶3∶2
2. 2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化CO氧化反应的模型进行了深入研究。下列关于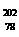 Pt的说法正确的是 ( )
Pt的说法正确的是 ( )
A.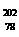 Pt和
Pt和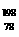 Pt的质子数相同,互称为同位素
Pt的质子数相同,互称为同位素
B.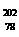 Pt和
Pt和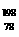 Pt的中子数相同,互称为同位素
Pt的中子数相同,互称为同位素
C.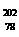 Pt和
Pt和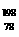 Pt的核外电子数相同,是同一种核素
Pt的核外电子数相同,是同一种核素
D. 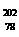 Pt和
Pt和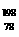 Pt的质量数不同,不能互称为同位素
Pt的质量数不同,不能互称为同位素
3 M 2+离子有2个电子层,则M在周期表的位置是 ( )
A.第二周期零族 B.第二周期Ⅷ族 C.第二周期ⅡA族 D.第三周期ⅡA族
1.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是 ( )
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
11、(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3- +4H++3e- = NO+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:____________________________________。
(2)反应中硝酸体现了____ 、_______ 性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是 mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
。
10、(11分)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3- 六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子_________、_______、_____________。乙厂的废水中含有另外三种离子。
对于该两厂的废水,可采取下列两种方法来处理。 www.k@s@5@ 高#考#资#源#网
(1)如果在废水中加一定量 (选填:活性炭或铁粉),可以发生 反应,离子方程式是 ,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:
____________________;
____________________。
经过滤后的废水主要含 ,可用来浇灌农田。
9. (6分)某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式 。
(2)实验②中化学反应转移电子的物质的量是 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是_________________。
8、(13分)某无色溶液,其中可能存在的离子有:Na+、Ag+、Fe3+、Ba2+、Al3+、AlO2-、S2-、SO32-、SO42-,现取该溶液进行A、B、C三步实验,实验结果如下:


(1)至实验A完成为止,分析题给信息:
①由“无色溶液”可以得出的结论: _____________________________________________
______________________________________________。
②由有“气体甲”和“淡黄色沉淀甲”生成可以得出的结论: ____
__________________________________________________________。
③气体甲的成分有哪几种可能,答:a: ___、b:_____________________、
c: _________。(有多少种就填多少种,可不填满。)
(2)沉淀乙是 (填化学式),由溶液甲生成沉淀乙的离子方程式为__________________________________________。
(3)沉淀丙可能是 (填化学式)。
(4)综合上述信息,可以肯定存在的离子有 。
7、常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+下列说法不正确的是( )
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱
B.在H2O2分解过程中,溶液的PH不变
C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
D.H2O2生产过程要严格避免混入Fe2+
6、lO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4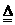 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
( )
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
( )
A.KClO3在反应中失去电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.1 molKClO3参加反应有2mol电子转移
5、、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转换关系(未配平):
① G → Q + NaCl
② Q +
H2O 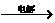 X
+ H2
X
+ H2
③ Y + NaOH → G+ Q+H2O ④ Z + NaOH → Q + X + H2O
这五种化合物中,氯的化合价由低到高的顺序为( )
A.G、Y、Z、Q、X B.Z、X、G、Y、Q
C.Q、G、Z、Y、X D.G、Y、Q、Z、X www.k@s@5@ 高#考#资#源#网
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com