
题目列表(包括答案和解析)
33.(8分)某含有一个双键的气态烯烃和另一气态烷烃的混合气体,在同温同压下其密度是H2的13.2倍。在标准状况下将4.48L混合气体通过足量的溴水,结果溴水增重3.36g。
⑴通过计算和分析判断混合气体由哪两种烃组成?
⑵写出该烯烃与溴水反应的化学方程式。
⑶求原混合气体中各烃的体积分数。
www.k@s@5@ 高#考#资#源#网
高一2009-2010学年第二学期期中考试
32.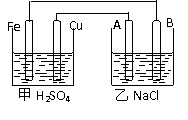 (13分)根据右图回答以下问题:(A、B均为碳棒)
(13分)根据右图回答以下问题:(A、B均为碳棒)
⑴甲池是 乙池是
且Fe极为 极,A极为 极
⑵A极的电极反应
发生 反应
⑶过一段时间后,甲池中pH值 (填增大、减小或不变)
⑷若甲池中Fe溶解0.1mol,则乙池中产生气体的总体积(标准状况)为 L
⑸若上述条件不变,乙池中改为AgNO3溶液, 极质量会增加 g
31.(7分)化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下图所列装置是用燃烧法确定有机物分子式常用的装置。
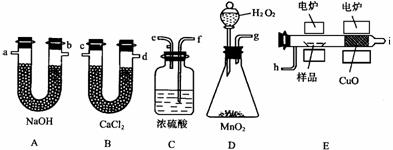
回答下列问题:
⑴产生的氧气按从左到右流向,所选装置各导管的连接顺序是 [来源:]
⑵C装置中浓H2SO4的作用是
⑶D装置中MnO2的作用是
⑷燃烧管中CuO的作用是
⑸若准确称取0.42g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后
A管质量增加1.32g,B管质量增加0.54g,则该有机物的最简式为
30.(15分)A、B、C、D四种短周期元素的原子序数依次增大,A、D同主族,B、C同周期,
它们形成的化合物如图,请回答下列问题:
|
甲 |
乙 |
丙 |
丁 |
戊 |
|
A︰B=4︰1] |
A︰C=1︰1 |
A︰C=2︰1 |
D︰C=1︰1 |
D︰C=2︰1 |
|
气态 |
液态 |
液态 |
固态 |
固态 |
⑴写出下列元素名称 A B D
⑵写出C元素在元素周期表中的位置第 周期 族
⑶甲的结构式 丁的电子式
⑷乙属 晶体
⑸B元素的最高价氧化物跟丁反应的化学方程式
在该反应中转移电子数为
⑹若已知25℃,101kPa下,lg甲完全燃烧放出55.6kJ热量,则该反应的热化学方程式是
⑺若A的单质形成燃料电池(KOH溶液为电解质溶液),写出负极电极反应式
29.( 11分)
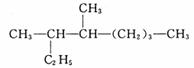 ⑴某有机物结构简式如右图所示,
⑴某有机物结构简式如右图所示,
其名称是 ,
它的一溴代物有 种同分异构体[
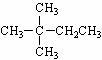
⑵ 由某烯烃与H2加成反应制得,写出该烯烃的结构简
式 ,其名称是
⑶写出主链上有五个碳原子,支链上有一个甲基、一个乙基的烷烃所有同分异构体的结构
简式
28.已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1 mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
www.k@s@5@ 高#考#资#源#网
第II卷(非选择题 共54分)
27.在一定温度下,把3.0moLM和2.5moLN混合于2.0L的密闭容器中,发生反应的化学方程式为:3M(g)+N(g) XP(g)+2Q(g) ,5min后反应达到平衡,容器内的压强变小,已知Q的平均反应速率为0.10 mol·L-1·min-1,下列说法错误的是( )
XP(g)+2Q(g) ,5min后反应达到平衡,容器内的压强变小,已知Q的平均反应速率为0.10 mol·L-1·min-1,下列说法错误的是( )
A.X的值为1 B.M的平均反应速率为0.15 mol·L-1·min-1
C.M的转化率为60% D.平衡时P的浓度为0.25 mol·L-1
26.有A、B、C、D四种金属,若将B放入A的硫酸盐溶液中,B的表面有A析出; C、D分别浸入稀硫酸中,C生成氢气的速率更大;用A作电极电解氯化铜溶液时,氯化铜溶液浓度不变; B与D用导线相连插入稀硫酸中,电子由D极经导线流向B极。则这四种金属的活动性由强至弱的顺序为( )
A.A>B>C>D B.C>D>B>A C.C>A>D>B D.B>D>C>A
25.银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O、Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。下列说法中错误的是( )
A.原电池放电时,负极上发生反应的物质是Zn
B.溶液中OH-向正极移动,K+、H+向负极移动
C.工作时,负极区溶液pH减小,正极区pH增大
D.负极上发生的反应是Zn+2OH--2e-=Zn(OH)2
24.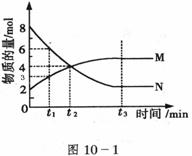 在一定温度下,容器内某一反应中M、N的物质的量
在一定温度下,容器内某一反应中M、N的物质的量
随反应时间变化的曲线如图10-1,下列表述中正确
的是( )
A.反应的化学方程式为:2 M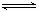 N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com